Majalah Farmasetika, 11 (1) 2026, 57-69
https://doi.org/10.24198/mfarmasetika.v11i1.68826
Artikel Penelitian
Prodio Efa Gaharani*1, Taofik Rusdiana2 , Ikhsan Rambia2
1Program Studi Profesi Apoteker, Fakultas Farmasi, Universitas Padjadjaran, Sumedang, Jawa Barat, Indonesia 45363
2Fakultas Farmasi, Universitas Padjadjaran, Sumedang, Jawa Barat, Indonesia 45363
*E-mail : prodio21001@mail.unpad.ac.id
(Submit 18/12/2025, Revisi 23/12/2025, Diterima 26/12/2025, Terbit 25/01/2026)
Abstrak
Kualitas obat sangat dipengaruhi oleh mutu bahan baku sehingga proses seleksi pemasok bahan baku obat menjadi poin kritis dalam pemenuhan CPOB dan pengendalian rantai pasok. Kasus cemaran etilen glikol (EG) dan dietilen glikol (DEG) yang ditemukan BPOM menunjukkan kegagalan dalam kualifikasi pemasok khususnya seleksi pemasok sehingga berdampak langsung bagi keamanan pasien. Penelitian ini bertujuan untuk mengembangkan formulir seleksi pemasok bahan baku obat khususnya di PT. XYZ yang mengacu pada regulasi di Indonesia sebagai langkah antisipatif terhadap risiko mutu. Penelitian ini menggunakan pendekatan kualitatif deskriptif dengan pengembangan formulir. Pengembangan ini dilakukan melalui kajian sistematis terhadap CPOB, Surat edaran BPOM Nomor 5 tahun 2023, Regulasi BPOM, APIC (Active Pharmaceutical Ingredients Commite), dan literatur yang relevan dengan parameter yang disusun berdasarkan prinsip risk based approach sesuai ICH Q9. Hasil penelitian menunjukkan formulir seleksi pemasok harus mencangkup verifikasi legalitas dokumen, pemeriksaan mutu dan ketertelusuran rantai pasok. Formulir seleksi pemasok ini dapat menjadi salah satu upaya yang efektif bagi Industri Farmasi dalam membuat sistem yang lebih terukur dan terdokumentasi sehingga meningkatkan pengendalian mutu bahan baku obat. Selain diimplementasikan di PT. XYZ, formulir ini berpotensi menjadi acuan bagi Industri Farmasi khususnya di Indonesia dalam memperkuat pengendalian mutu bahan baku obat dan mencegah terulangnya insiden substandard seperti kasus cemaran EG dan DEG.
Kata kunci: Bahan Baku Obat, Pengendalian Mutu, Rantai Rasok (supply chain), Seleksi Pemasok,
Teks Lengkap:
Pendahuluan
Pendahuluan
Peningkatan kualitas hidup masyarakat dapat dilakukan salah satunya dengan penyediaan obat yang memiliki keamanan, khasiat dan mutu yang baik. Obat bermutu tinggi sangat dipengaruhi oleh mutu bahan baku obat yang digunakan, obat dengan mutu tersebut dapat menghasilkan efek terapeutik yang optimal dengan efek samping yang rendah atau tidak menimbulkan bahaya tambahan (1). Sebaliknya, obat yang memiliki mutu rendah maka dapat menyebabkan kegagalan terapi, resistensi mikroba bahkan kematian (2).
Standar mutu internasional seperti Good Manufacturing Practice (GMP) menjadi acuan global yang telah diterapkan secara meluas untuk memastikan konsistensi, keamanan, dan efektivitas suatu produk sepanjang proses. Namun, implementasi standar global ini menjadi tantangan tersendiri bagi negara berpenghasilan menengah seperti Indonesia berupa keterbatasan finansial, infrastruktur yang kurang memadai, regulasi yang tidak efisien atau lemah, fasilitas yang terbatas, proses produksi dan kurangnya pelatihan serta pengawasan internal (3). Keterbatasan tersebut menuntut industri untuk menerapkan regulasi nasional berupa Cara Pembuatan Obat yang Baik dan Benar (CPOB) dengan regulator Badan Pengawas Obat dan Makanan (BPOM), termasuk persyaratan kualifikasi pemasok bahan obat yang semakin ketat (4). Sejalan dengan itu, WHO menegaskan bahwa sistem jaminan mutu dan pengawasan distribusi obat yang kuat dapat menjamin tidak beredarnya obat palsu dan substandar di pasar, maka bahan baku obat dari mulai pemasok hingga distribusi harus dipantau secara ketat sesuai dengan regulasi Indonesia yang berjalan (5). Selain itu, CPOB 2024 menekankan ketertelusuran rantai pasok upaya dalam mempermudah pelacakan dari asal usul bahan dan memastikan mutu terbaik sehingga temuan bisa dicegah sejak sumbernya bukan setelah produk jadi.
Dalam pemenuhan syarat obat aman, berkhasiat dan bermutu maka sebuah industri farmasi harus menerapkan supply chain management (SCM) yang baik dan ketat. SCM memastikan seluruh proses dari hulu (upstream) hingga ke hilir (downstream) dimana proses dimulai dari pengadaan bahan baku, proses produksi, distribusi hingga obat sampai dipakai oleh pasien yang berpotensi dalam mempengaruhi kualitas akhir produk (6). Oleh karena itu, kualifikasi pemasok khususnya seleksi pemasok menjadi komponen krusial dalam penerapan SCM di Industri farmasi, pemasok yang tidak terkualifikasi berpotensi meningkatkan risiko produk.
PT. XYZ sebagai salah satu industri farmasi nasional telah memiliki sistem seleksi pemasok bahan baku obat yang cukup baik mencangkup dokumen mutu, evaluasi mutu bahan baku obat, dan verifikasi dokumen legalitas termasuk Certificate of Analysis (CoA) dan CPOB atau dokumen setara. Sistem ini menunjukkan bahwa PT. XYZ telah menerapkan prinsip seleksi pemasok yang tercantum dalam Surat edaran BPOM Nomor 5 tahun 2023 tentang Kualifikasi Pemasok Bahan Obat (7). Implementasi seleksi pemasok di PT. XYZ masih menunjukkan variasi antar industri meskipun regulasi sudah ada. PT. XYZ masih berfokus pada proses seleksi awal saja dan belum sepenuhnya mencangkup aspek ketertelusuran rantai pasok (traceability), verifikasi asal bahan dan sistem pemantauan mutu selama distribusi bahan. Kondisi yang sama juga terjadi pada berbagai industri farmasi di negara berkembang, di mana proses pemantauan dalam rantai pasok umumnya belum terhubung secara optimal dengan penerapan manajemen risiko mutu yang baik (8). Wickett et al (2022) menegaskan bahwa kelemahan rantai pasok di industri farmasi disebabkan oleh kurangnya koordinasi antara pemasok, produsen, dan distributor sehingga dapat meningkatkan risiko bahan baku obat substandar atau tidak terkualifikasi masuk ke proses produksi meningkat (9). Berdasarkan kajian terhadap regulasi di Indonesia terdapat beberapa kesenjangan kritis seperti implementasi seleksi pemasok yang bervariasi dan tidak seragam di Industri dan fokus seleksi hanya pada aspek legalitas awal tanpa penilaian terhadap rantai pasok. Dengan demikian, diperlukan kajian untuk mengevaluasi proses seleksi pemasok baik produsen maupun distributor baru di PT. XYZ yang menyeluruh dan terdokumentasi dengan baik untuk memastikan kepatuhan terhadap CPOB dan CDOB secara konsisten, dengan pengembangan formulir seleksi pemasok.
Metode
Penelitian ini menggunakan pendekatan kualitatif deskriptif dengan berbasis dokumen sebagai respon untuk memperkuat implementasi regulasi yang semakin ketat dan sebagai pemenuhan kebutuhan akan alat pemilihan pemasok yang sistematis dan terdokumentasi di tingkat Industri Farmasi. Studi awal dilakukan melalui kajian sistematis terhadap pedoman resmi seperti CPOB, Surat edaran BPOM Nomor 5 tahun 2023, Regulasi BPOM, dan APIC (Active Pharmaceutical Ingredients Commite)(10,7,11). Selain itu, terdapat jurnal ilmiah kredibel 10 tahun terakhir dan dokumen internal PT. XYZ terkait seleksi pemasok. Kajian ini memetakan setiap persyaratan regulasi dengan kebutuhan operasional perusahaan untuk menemukan kesenjangan (gap) dan poin-poin kritis bagi produsen dan distributor baru. Hasilnya dirancang menjadi Formulir seleksi pemasok baik produsen atau distributor baru sehingga dapat direkomendasikan untuk menjadi acuan dalam seleksi pemasok bagi Industri Farmasi khususnya di Indonesia.
Hasil dan Pembahasan
Temuan BPOM terkait dengan kandungan Etilen Glikol (EG) dan Dietilen Glikol (DEG) menunjukkan bahwa risiko keamanan obat dapat berasal dari mutu bahan baku obat salah satunya pelarut. Meskipun secara regulasi pelarut diperbolehkan, namun potensi EG dan DEG dapat meningkat ketika bahan baku obat tidak sesuai persyaratan Badan POM dan dipasok dari produsen atau distributor yang tidak terkualifikasi dengan baik (12). Dalam hasil pengawasan BPOM menemukan bahwa beberapa produk sirup dengan EG melebihi ambang batas dan berasal dari Pedagang Besar Farmasi, Instalasi Farmasi Pemerintah, Apotek, Instalasi Farmasi Rumah Sakit, Puskesmas, Klinik, Toko Obat, dan praktik mandiri tenaga kesehatan. Dalam temuan kasus ini menegaskan atas pentingnya seleksi pemasok yang ketat, dan menunjukkan bahwa kelemahan rantai pasok bahan baku obat mempengaruhi keamanan produk secara langsung sehingga mendorong regulator untuk mengambil tindakan tegas seperti recall, penghentian distribusi hingga sanksi administrasi terhadap pihak pemasok yang melanggar aturan (13).
Berdasarkan temuan BPOM mengenai kasus cemaran EG dan DEG, PT. XYZ perlu meningkatkan dan mengantisipasi pengawasan mutu bahan baku obat melalui pengembangan formulir seleksi pemasok bahan baku obat sebagai langkah antisipatif. Formulir ini dirancang untuk memastikan setiap produsen dan distributor baru yang akan memasok bahan baku obat telah melalui verifikasi yang menyeluruh sebelum disetujui. Pada PT. XYZ telah terdapat seleksi pemasok, akan tetapi formulir seleksi pemasok dari produsen dan distribusi menjadi satu sehingga berpotensi menimbulkan ketercampuran data dan ketidaktepatan dalam penilaian produsen atau distributor yang akan di memasok, formulir dapat dilihat pada Tabel 2. Pembaruan dari formulir ini dilakukan untuk memisahkan dan memperjelas parameter seleksi sesuai dengan regulasi sehingga menghasilkan formulir yang lebih terstuktur, akurat dan sesuai dengan pendekatan berbasis risiko. Seleksi pemasok bahan baku obat dilakukan pada:
Tabel 2 Formulir Seleksi Pemasok (Sebelum Perubahan)

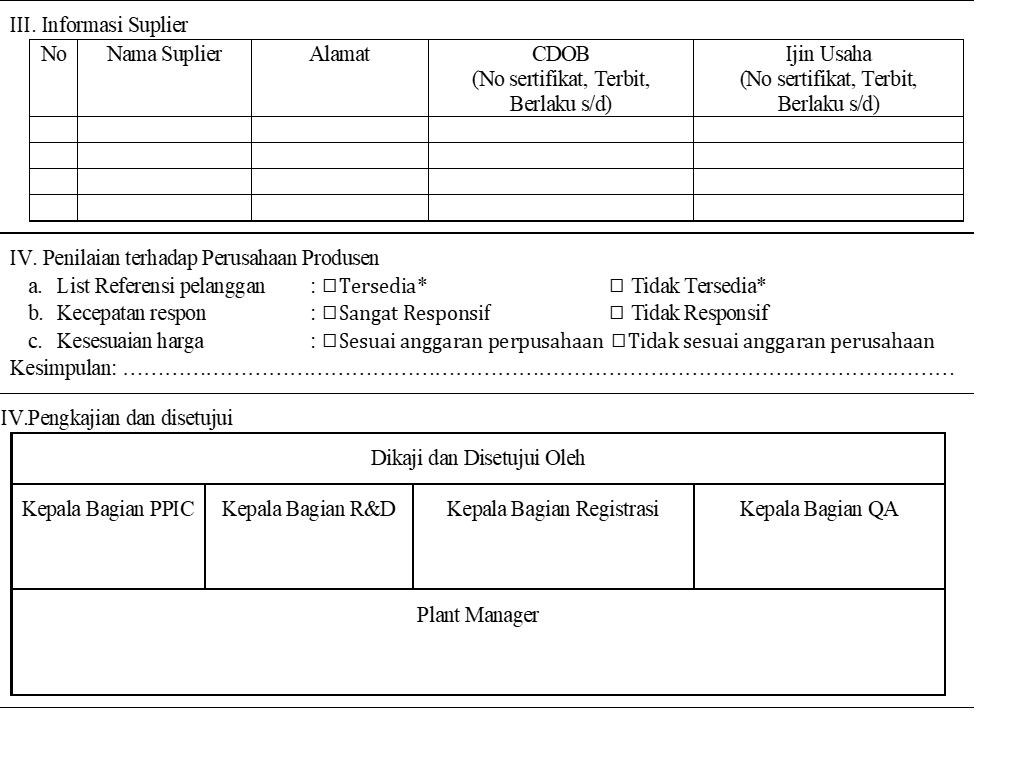
Produsen Baru
Kasus temuan EG dan DEG dari BPOM memperkuat urgensi pemilihan produsen yang memiliki rekam jejak kepatuhan terhadap pemenuhan mutu yang baik. Seleksi bahan baku obat dari produsen baru dimulai dari penilaian terhadap kapabilitas fundamental dan kepatuhan terhadap regulasi yang mengarahkan industri farmasi untuk memverifikasi identitas produsen, status dokumen sistem mutu berupa legalitas dokumen seperti sertifikat CPOB, GMP maupun dokumen yang setara serta CoA untuk indikator utama kredibilitas dan keberlanjutan pemasok (14). Legalitas dokumen bukan hanya alat administratif tetapi memastikan kepatuhan terhadap regulasi mutu dan keamanan produk kelengkapan dokumen lain seperti TSE/BSE (Transmissible Spongiform Encephalopathy/ Bovine Spongiform Encephalopathy, untuk bahan yang bersumber dari hewan harus diverifikasi sejak dini untuk memitigasi risiko (15).
Selain itu, bahan baku obat dari produsen dapat berpotensi membawa risiko lebih tinggi sehingga proses seleksi harus menerapkan risk based approach yakni mengklasifikasikan risiko pemasok berupa kritis, mayor, dan minor yang dapat dilihat pada Tabel 1 (16). Khususnya bahan klasifikasi kritis harus melalui pengujian dan pemeriksaan dokumen seperti MSDS (Material Safety Data Sheet) dan DMF (Drug Master File) yang dilakukan secara ketat. Bahan baku obat yang bersumber dari produsen baru harus melalui pemeriksaan hasil mutu mencangkup pemeriksaan sampel dan hasil trial seperti kemurnian, stabilitas dan kesesuaian terhadap Farmakope (17).
Tahapan akhir, pada hasil seleksi produsen baru akan dikaji oleh bagian bagian yang berkaitan seperti Kepala Bagian Research and Development (R&D), Purchasing, Quality control (QC). Selanjutnya, akan disetujui oleh bagian Quality Assurance (QA) dan Plant Manager. Hal ini untuk menjamin bahwa pemasok yang disetujui sudah memenuhi persyaratan sesuai CPOB dengan mutu yang terjamin. Setelah pemasok bahan baku obat dari produsen baru dikaji dan disetujui maka akan mendapat kode produsen dan bahan baku obat. Formulir seleksi pemasok produsen baru dapat dilihat pada Tabel 3.
Tabel 3 Formulir Seleksi Pemasok Produsen Baru (Setelah Perubahan)

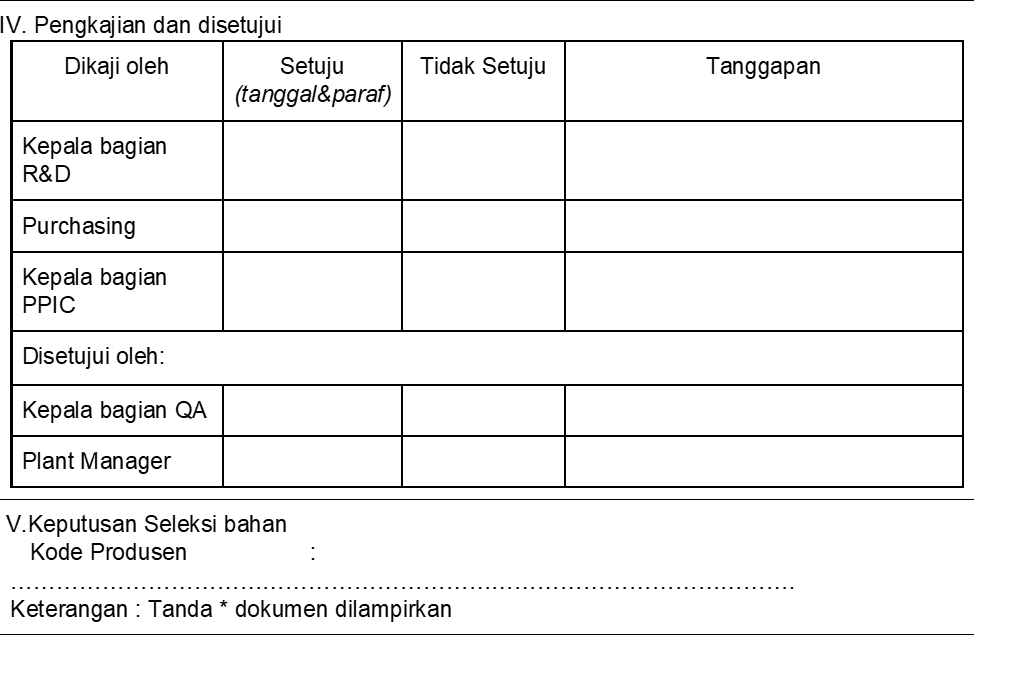
Distributor Baru
Seleksi bahan baku obat dari distributor baru dimulai dengan verifikasi identitas dan legalitas distributor mencangkup CDOB, NIB, NPWP, dan SIPA Apoteker Penanggung jawab untuk menjamin keabsahan dan kepatuhan terhadap distribusi obat. Informasi bahan baku obat berisi data terkait bahan baku obat, identitas dan asal produsen, serta pola pembelian langsung maupun tidak langsung dimana informasi ini digunakan untuk menilai keaslian bahan, menelusuri integritas rantai pasok, dan memastikan kepatuhan terhadap standar internasional yang relevan seperti CDOB (Cara Distribusi Obat yang Baik), Good Distribution Practice (GDP) atau Letter of Authorization (LoA). CDOB atau GDP menjadi salah satu indikator krusial bahwa distributor memiliki sistem yang terkendali dalam menjamin mutu bahan baku obat selama penyimpanan dan transportasi mencangkup suhu, keamanan dan dokumentasi yang memadai.
Selain itu, rantai pasok menjadi sorotan khusus dalam seleksi distributor baru mengingat ditemukannya kasus EG & DEG oleh BPOM. Rantai pasok yang jelas memudahkan ketertelusuran bahan baku obat. Ketertelusuran rantai pasok dapat meningkatkan pengawasan dan visibilitas terutama pada rantai pasok yang kompleks dan panjang. Hal ini mempermudah industri farmasi dalam memperoleh secara real time mengenai pihak yang terlibat dalam proses produksi, jenis dan asal bahan yang digunakan, waktu pembuatan, serta lokasi setiap tahapan distribusi. Ketertelusuran rantai pasok ini memungkinkan identifikasi cepat ketika terjadi penyimpangan dan memastikan seluruh proses berjalan sesuai dengan standar mutu dan regulasi yang berlaku (18). Ketertelusuran rantai pasok telah diperjelas dalam surat edaran BPOM nomor 5 tahun 2023 tentang Kualifikasi Pemasok Bahan Obat yang menindaklanjuti kasus EG/DEG. Dalam surat edaran terdapat hal-hal yang perlu diperhatikan, antara lain:
a.Pemasok bahan obat harus diperoleh dari pemasok yang memiliki sertifikat CPOB
untuk industri farmasi bahan obat dan sertifikat CDOB untuk PBF bahan Obat
b.Pemasok bahan obat atau tambahan obat memiliki bahan obat standar
pharmaceutical grade
c.Pemasok yang berasal dari luar negeri memiliki GMP atau dokumen setara yang
dikeluarkan oleh otoritas pengawas obat negara lain, memiliki sertifikat GDP atau
dokumen setara, distributor yang ditunjuk oleh dan/atau bekerja sama dengan
produsen bahan obat dan distributor yang memiliki kerjasama dengan distributor
yang ditunjuk oleh produsen bahan obat dibuktikan dengan dokumen
penunjukan/kerjasama dalam rantai pasoknya hingga produsen bahan obat.
d.Industri farmasi harus memprioritaskan pasokan bahan baku obat langsung dari
pabrik aslinya, jika terpaksa menggunakan distributor maka dipastikan distributor
tersebut mendapatkan barang secara langsung dari pabrik atau dari distributor
yang ditunjuk oleh pabrik luar negeri (rantai pasokan harus pendek).
e.Pemasok harus mampu menyediakan informasi yang berkesinambungan dengan
aspek keamanan dan/atau pemastian terhadap keaslian bahan obat.
Dalam CPOB 2024 menyatakan Industri Farmasi harus memastikan keterlibatan distributor bahan awal luar negeri dan/atau PBF dalam rantai pasok sebagai upaya dalam memastikan integritas dan ketertelusuran rantai pasok. Berikut adalah perolehan bahan awal yang dilaksanakan berdasarkan prioritas dengan urutan,
a.Diperoleh langsung dari pabrik pembuat bahan awal
b.Diperoleh dari PBF
c.Diperoleh dari distributor luar negeri yang ditunjuk oleh dan/atau bekerja sama
dengan pabrik pembuat bahan awal
d.Diperoleh dari distributor luar negeri yang memiliki kerjasama dengan distributor
yang ditunjuk langsung oleh pabrik pembuat bahan awal.
Dalam pemenuhan ketertelusuran rantai pasok yang baik dan jelas terdapat beberapa tantangan seperti kurangnya transparansi dan kepercayaan antar pemangku kepentingan sehingga meningkatkan risiko bahan obat terkontaminasi (termasuk kasus temuan EG/DEG), ketidakpastian dalam menyediakan bahan baku obat yang berkualitas dalam jumlah dan waktu yang diperlukan, harga yang terbatas sehingga mempengaruhi kualitas produk dan daya saing, dan perbedaan regulasi antar negara sehingga sistem ketertelusuran diatur berbeda oleh badan regulator (seperti DSCSA di Amerika Serikat, FMD di Eropa, CDSCO di India dan BPOM di Indonesia) (18, 19). Untuk menghadapi tantangan tersebut diperlukan regulasi baik nasional dan internasional terkait ketertelusuran rantai pasok agar keamanan pasokan bahan baku obat dapat memenuhi mutu, keamanan dan khasiat yang baik. Salah satunya dengan pembuatan formulir seleksi pemasok distributor baru dengan mencantumkan rantai pasok yang jelas, formulir dapat dilihat pada Table 4.
Tabel 4 Formulir Seleksi Pemasok Distributor Baru (Setelah Perubahan)
| SELEKSI PEMASOK DISTRIBUTOR BARU |
| I. Informasi Distributor a. Nama distributor : …………………………………………………………………………………………. b. Alamat Gudang : …………………………………………………………………………………………. c. Alamat Head Office : …………………………………………………………………………………………. d. No.telp/Fax/Email : …………………………………………………………………………………………. e. Status produsen : ◻sudah terkualifikasi ◻belum terkualifikasi f. Dokumen legalitas : ◻CDOB* : ……………. Masa berlaku : ………..………. s/d…………………. ◻ NIB* : ……………. Masa berlaku : ..……………… s/d…………………. ◻ NPWP* : ……………. Masa berlaku : …..……….….. s/d………………… ◻ SIPA APJ : ◻Ada ◻ Tidak ada No SIPA : ……………………………… |
| II. Informasi Bahan Baku a. Nama Bahan Baku : …………………………………………………………………………………………. b. Jenis Bahan Baku : ◻ Zat aktif ◻ Eksipien c. Nama Produsen : …………………………………………………………………………………………….. d. Alamat Produsen : ……………………………………………………………………………………………. e. Status Bahan Baku : ◻ Bahan baku baru ◻ Bahan Baku Terdaftar/existing (jika bahan baku baru maka lanjut pengisian Form Seleksi Produsen Baru) f.Jenis Pembelian i. Langsung : ◻ LoA* Tanggal : ………………………………………… Ii. Tidak langsung a. Nama produsen (rantai 2) : ……………………………………………. b. Alamat produsen (rantai 2) : …………………………………………… c. Dokumen legalitas (rantai 2) : ◻ Izin Usaha* ◻ GDP (jika ada)* ◻ LoA produsen – Rantai 1 ……………………………………………….. Dok lain (bukti pengiriman)*………………………………………………………….. ◻ LoA Rantai 1 – Rantai 2 ………………………………………………. Dok lain (bukti pengiriman)*………………………………………………………….. g.Hasil Audit pemasok :…………………………………………. Tanggal Audit : ………………………….. h.Riwayat Audit : ◻ BPOM ◻ WHO ◻ FDA ◻ lembaga lain …….. Keterangan : Tanda * dokumen dilampirkan |

Klasifikasi pemasok bahan baku menjadi salah satu peran penting dalam memastikan produk memenuhi persyaratan yang telah ditentukan serta keberlanjutan rantai pasok. Klasifikasi ini membantu Industri Farmasi dalam menilai dan mengelompokkan pemasok berdasarkan kinerja, reliabilitas dan kepatuhan terhadap standar seperti CPOB ataupun GMP. Tabel 1 memperlihatkan klasifikasi risiko pemasok yang digunakan di PT. XYZ,
Tabel 1 Klasifikasi Risiko Pemasok
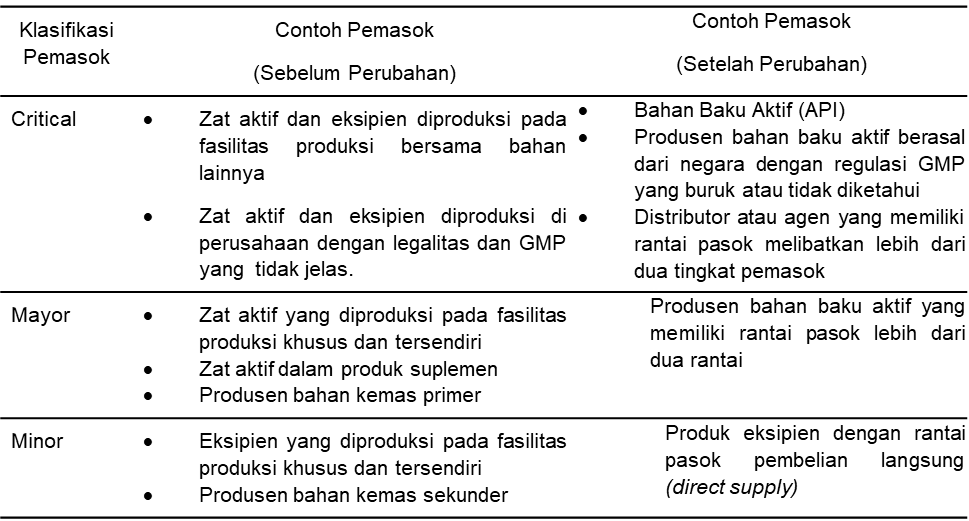
Dalam konteks Industri Farmasi pengelompokkan sesuai dengan Tabel 1 menjadi penting karena bahan baku obat yang digunakan dapat secara langsung mempengaruhi mutu obat. Klasifikasi risiko pemasok dibagi menjadi 3 klasifikasi yaitu critical, mayor dan minor yang mempresentasikan tingkatan risiko dari tinggi ke rendah. Hal ini sejalan dengan berbagai penelitian yang menekankan pentingnya klasifikasi pemasok berbasis risiko untuk memperkuat ketahanan rantai pasok. Selain itu, klasifikasi pemasok menjadi critical-risk, medium risk, dan low risk merupakan penerapan langsung dari prinsip ICH Q9 (16). Pada high risk suppliers di klasifikasikan untuk bahan baku yang berdampak langsung pada kualitas produk atau keselamatan pasien seperti zat aktif sehingga diperlukan audit. Medium high-risk suppliers diperuntukkan bagi pemasok eksipien non kritis yang bukan digunakan untuk formulasi sediaan steril dan penyedia layanan kalibrasi . Selain itu, untuk low risk bagi pemasok dengan pengaruh minimal terhadap kualitas seperti penyedia alat tulis atau barang habis pakai umum (20,21). Klasifikasi risiko pemasok pada PT. XYZ menegaskan pentingnya ketertelusuran rantai pasok dari distributor penyedia bahan baku obat serta pemenuhan regulasi pada produsen mengingat kasus cemaran EG & DEG berasal dari produsen dengan pemenuhan GMP yang lemah.
Regulasi di Indonesia dalam hal CPOB 2024 dan Surat Edaran BPOM Nomor 5 tahun menunjukkan bahwa proses seleksi yang sistematis dan terdokumentasi menjadi langkah antisipatif dalam menjamin mutu, konsistensi, dan kepatuhan terhadap regulasi khususnya rantai pasok industri farmasi. Formulir yang telah dibuat menegaskan produsen atau distributor baru harus melalui penilaian baik legalitas, kualitas bahan, dan reliabilitas pasok. Hal ini dilakukan untuk memastikan keputusan yang diambil bersifat objektif, terukur dan sesuai dengan kebutuhan masing-masing industri farmasi. Selain itu, proses ini terbukti mampu mengurangi risiko jangka panjang terhadap gangguan pasokan, ketidaksesuaian mutu, dan kepatuhan regulasi serta mencegah ancaman keselamatan terhadap Masyarakat (22). Implementasi formulir seleksi pemasok tidak hanya menjadi alat administrasi, tetapi berperan dalam pengendalian mutu untuk mendukung terciptanya obat yang aman, berkhasiat dan bermutu dengan rantai pasok yang tertelusur.
Kesimpulan
Seleksi pemasok menjadi proses kritis dalam menjadi mutu obat. Kajian ini menunjukkan bahwa PT. XYZ telah memiliki proses seleksi pemasok, namun implementasinya masih sebatas verifikasi awal dan belum mencangkup ketertelusuran rantai pasok, verifikasi asal bahan serta pengendalian mutu selama distribusi. Regulasi nasional seperti CPOB, Surat edaran BPOM Nomor 5 tahun 2023, Regulasi BPOM, serta acuan pendukung Internasional seperti GMP dan APIC (Active Pharmaceutical Ingredients Commite) menekankan pentingnya seleksi pemasok dimulai dari verifikasi legalitas dokumen, pemeriksaan mutu dan ketertelusuran rantai pasok. Temuan kasus cemaran EG/DEG menegaskan pentingnya penerapan risk based approach terhadap pemasok untuk mencegah masuknya bahan baku obat yang tidak memenuhi standar dari produsen atau distributor yang tidak terkualifikasi. Dengan demikian, penelitian ini menghasilkan formulir seleksi pemasok produsen dan distributor baru sebagai alat yang sistematis dan terdokumentasi dalam meningkatkan kepatuhan PT. XYZ terhadap regulasi terbaru dalam memperkuat pengendalian mutu. Formulir seleksi ini dapat menjadi acuan bagi industri farmasi lainnya dalam memperkuat sistem seleksi pemasok guna menjamin produk aman, berkhasiat dan bermutu sesuai dengan regulasi yang berlaku.
Daftar Pustaka
1. World Health Organization. WHO good manufacturing practices for pharmaceutical products: main principles. Dalam WHO Technical Report Series, No. 986, Annex 2 [diunduh 3 Januari 2026]. Tersedian dari: https://cdn.who.int/media/docs/default-source/medicines/norms-and-standards/guidelines/inspections/trs986annex2.pdf?sfvrsn=320c9e62_6&download=true.
2. Sigalingging, O. S. dan Musfiroh, I. Analisis Kualifikasi Pemasok Obat di Salah satu Pedagang Besar Farmasi (PBF) di Kota Bandung. Majalah Farmasetika. 2022;7(5):469-477.
3. Chejor, P., Dorji, T., Dema, N., & Stafford, A. Good Manufacturing Practice in Low‐ and Middle‐Income Countries: Challenges and Solutions for Compliance. Public Health Chall. 2024; 3(1): 1-4.
4. Annisa, V. Kajian Penerapan Good Manufacturing Practice (GMP) di Industri Farmasi Indonesia. Majalah Farmasetika. 2024; 9(4): 351-366.
5. World Health Organization. Substandard and Falsified Medical Products [diunduh 5 Desember 2025]. Tersedia dari: https://www.who.int/en/news-room/fact-sheets/detail/substandard-and-falsified-medical-products.
6. Rachbini, W. J. Supply Chain Management dan Kinerja Perusahaan. Journal of Bussines and Banking. 2016; 7(1).
7. BPOM. Kualifikasi Bahan Obat [diunduh 4 Desember 2025]. Tersedia dari: https://jdih.pom.go.id/download/rule/1494/5/2023/Surat%20Edaran%20Kepala%20Badan%20Pengawas%20Obat%20dan%20Makanan%20Nomor%205%20Tahun%202023%20tentang%20Kualifikasi%20Pemasok%20Bahan%20Obat.
8. Chejor, P., Dorji, T., Dema, N., Stafford, A. Good Manufacturing Practice In Low- and Middle-Income Countries: Challenges and Solutions for Compliance. Int J Public Health Challenges. 2023; 1-4.
9. Wickett, E., Plumlee, M., Smilowitz, K., Phanouvong, S., Pribluda, V. Inferring Sources of Substandard and Falsified Products in Pharmaceutical Supply Chains [diunduh 7 Desember 2025]. Tersedia dari: https://arxiv.org/pdf/2207.05671
10. Badan Pengawas Obat dan Makanan Republik Indonesia. Peraturan Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 7 Tahun 2024 tentang Standar Cara Pembuatan Obat yang Baik. Jakarta: BPOM RI; 2024.
11. Active Pharmaceutical Ingredients Commite. Best Practices guide for Managing Suppliers of API Manufacturers Version 2. Eropa: CEFIC; 2024.
12. BPOM. Seri Buku Saku Penanganan Kasus Cemaran Etilen Glikol dan Dietilen Glikol (EG/DEG) Dalam Sirop Obat. Jakarta: Badan Pengawas Obat dan Makanan; 2023.
13. BPOM. Informasi Keempat Hasil Pengawasan BPOM Terhadap Sirup Obat yang Diduga Mengandung Cemaran Etilen Glikol (EG) dan Dietilen Glikol (DEG) [ diunduh 28 November 2025]. Tersedia dari: https://www.pom.go.id/penjelasan-publik/informasi-keempat-hasil-pengawasan-bpom-terhadap-sirup-obat-yang-diduga-mengandung-cemaran-etilen-glikol-eg-dan-dietilen-glikol-deg.
14. Sarasati, B. A., & Dachyar, M. Green Supplier Selection Using Fuzzy Approach of AHP and VIKOR – A Case Study in an Indonesian Pharmaceutical Company. Proceedings of the 11th Annual International Conference on Industrial Engineering and Operations Management Singapore March 7-11, 2021. Singapore; 2021.
15. Monika, S. & Balamuralidhara, V. Transmissible Spongiform Encephalopathy and its Regulations. Indian Journalof Pharmaceutical Education and Research. 2023; 57(1): 57-62.
16. International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH). Quality Risk Management Q9. Geneva: ICH; 2023.
17. Saravanan, D., Muthudoss, P., Khullar, P., Rosevenis, A. Vendor Qualification: Utilization of Solid State Characterization “Toolbox” to Assess Material Variability for Active Pharmaceutical Ingredient. Journal of Applied Pharmaceutical Science. 2019; 9(9): 1-9.
18. Machsus, A. L., & Holis, A. H. Ketelusuran Rantai Pasok Bahan Baku Farmasi Sebagai Upaya Peningkatan Kualifikasi dan Keamanan Pemasok. An-Najat: Jurnal Ilmu Farmasi dan Kesehatan. 2025; 3(1): 127-138.
19. Melia, E., English A., & Naughton, B. D. The Impact of Global Falsified Medicines Regulation on Healthcare Stakeholders in The Legitimate Pharmaceutical Supply Chain: A Systematic Review. Frontiers in Medicine. 2024; 11: 1-10.
20. USP. General Chapter <1083> Supplier Qualification. United States Pharmacopeia–National Formulary (USP–NF). Rockville, MD: United States Pharmacopeial Convention. 2024.
21. ISPE. Good Practice Guide: Supplier Quality Management. International Society for Pharmaceutical Engineering (ISPE) [ Diunduh 5 Januari 2026]. Tersedia dari: https://ispe.org/pharmaceutical-engineering/march-april-2022/supplier-qualification-program-key-raw-materials.
22. Emrouznejad, A., Abbasi, S., Sicakyuz, C. Supply Chain Risk Management: A Content Analysis-Based Review of Existing And Emerging Topics. Int J Supply Chain Analytics. 2023; 3: 1-21
cara mengutip artikel
https://jurnal.unpad.ac.id/farmasetika/rt/captureCite/68826/26983
 Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3
Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3

