Majalah Farmasetika, 11 (1) 2026, 23-36
https://doi.org/10.24198/mfarmasetika.v11i1.69580
Review Artikel
Prayoga Drajat Pangestu Salim4*, Sandra Megantara 2,Shofia Durin Maknun4
1Program Studi Profesi Apoteker, Fakultas Farmasi, Universitas Padjadjaran, Bandung 2Departemen Analisis Farmasi dan Kimia Medisinal, Fakultas Farmasi, Universitas Padjadjaran, Bandung 3Pusat Riset Jawa Barat Universitas Padjadjaran
4PT.Combiphar, Padalarang
*E-mail : Prayoga25001@mail.unpad.ac.id
(Submit 03/01/2026, Revisi 05/01/2026, Diterima 08/01/2026, Terbit 25/01/2026)
Abstrak
Industri farmasi diwajibkan untuk mematuhi pedoman Cara Pembuatan Obat yang Baik (CPOB) sebagai upaya menjamin mutu, keamanan, dan efektivitas produk, termasuk dalam pengelolaan sistem komputerisasi melalui penerapan Computerized System Validation (CSV). Kajian berkala terhadap sistem CSV dilakukan untuk memastikan bahwa sistem komputerisasi tetap berada dalam kondisi tervalidasi, beroperasi sesuai dengan tujuan penggunaannya, serta memenuhi ketentuan regulatori yang berlaku, seperti CPOB 2024, GMP Annex 11, USP <1058>, dan ISO/IEC 27001. Penelaahan mencakup aspek pengendalian perubahan (change control), penanganan penyimpangan (deviation review), tinjauan keamanan dan pengelolaan akses sistem, evaluasi audit trail, verifikasi mekanisme backup–restore, serta pemantauan kinerja dan keandalan sistem secara berkelanjutan. Hasil kajian menunjukkan tidak ditemukannya indikasi penyimpangan operasional, penurunan performa sistem, maupun risiko terhadap integritas dan keamanan data. Seluruh aktivitas pengelolaan perubahan dan pemeliharaan sistem dilaksanakan secara terencana, terdokumentasi, dan tervalidasi dengan baik, termasuk penerapan Disaster Recovery Plan (DRP) yang mendukung kesinambungan operasional. Selain itu, sistem komputerisasi telah memenuhi prinsip ALCOA+ (Attributable, Legible, Contemporaneous, Original, Accurate, Complete, Consistent, Enduring, dan Available), sehingga menjamin akurasi, keterlacakan, serta perlindungan data dari akses yang tidak sah. Secara keseluruhan, kajian ini menunjukkan bahwa sistem komputerisasi di industri farmasi dapat beroperasi secara andal dan stabil serta selaras dengan persyaratan CPOB, GMP, dan ISO/IEC 27001 dalam mendukung kegiatan produksi dan pengawasan mutu.
Kata kunci: Validasi, Computer Validasi System (CSV), Industri Farmasi,
Teks Lengkap:
Pendahuluan
Industri farmasi merupakan suatu entitas usaha yang memiliki izin resmi untuk memproduksi obat atau bahan obat sesuai dengan ketentuan yang diatur dalam perundang-undangan. Seluruh proses produksi obat dan bahan obat di industri ini wajib mengikuti pedoman Cara Pembuatan Obat yang Baik (CPOB). Pedoman ini bertujuan untuk menjamin bahwa produk farmasi yang dihasilkan memiliki mutu tinggi, aman digunakan, dan efektif. Untuk mencapai standar kualitas tersebut, diperlukan pengendalian terhadap berbagai elemen seperti bahan baku, proses produksi, peralatan, serta kondisi lingkungan. Selain itu, pengawasan juga diperlukan untuk memastikan bahwa seluruh aspek tersebut memenuhi spesifikasi yang telah ditentukan. Dalam hal proses produksi, agar mutu produk tetap stabil dan berkualitas, sistem berjalan dengan baik diperlukan sistem validasi yang terkomputasi [1] .
Menurut peraturan bpom no 7 tahun 2024 Annex 7 sistem komputerisasi di industri farmasi adalah gabungan antara perangkat keras dan perangkat lunak yang bekerja bersama untuk menjalankan fungsi tertentu. Sistem ini digunakan untuk mendukung kegiatan produksi dan pengendalian mutu setelah melalui proses validasi. Dengan validasi tersebut, sistem mampu memastikan proses berjalan sesuai standar, menghasilkan data yang akurat dan konsisten, serta mengurangi risiko kesalahan manusia[1]. Validasi mencakup perangkat lunak, perangkat keras, jaringan, basis data, dan komponen pendukung lain yang berperan dalam operasional sistem [2].
Validasi sistem komputer merupakan rangkaian kegiatan terstruktur dan terdokumentasi yang memastikan setiap sistem berbasis komputer mampu berfungsi secara konsisten sesuai persyaratan fungsional, teknis, dan regulatori yang ditetapkan. Dalam industri farmasi, validasi memiliki peran strategis untuk menjamin keakuratan pemrosesan data, keandalan kinerja sistem, serta konsistensi operasional yang mendukung proses produksi, pengujian laboratorium, dan pengendalian mutu. Bukti objektif dari kegiatan validasi juga memastikan bahwa seluruh data elektronik yang dihasilkan bersifat akurat, dapat ditelusuri, dan bebas dari risiko kesalahan manual, sehingga integritas data tetap terjaga dan efektivitas sistem mutu semakin kuat [3].
Pelaksanaan validasi mengacu pada berbagai pedoman internasional seperti European Medicines Agency (EMA) Guidelines EudraLex Volume 4, Annex 11 Computerised Systems, yang diterbitkan tahun 2011 dan Food and Drug Administration (FDA) dalam Guidance for Industry Part 11 terkait Computerized System Validation (CSV), serta panduan industri seperti Risk-based Approach to Compliant GxP Computerized Systems (GAMP) 5 Edisi ke-2 Second Edition tahun 2022 yang memberikan kerangka kerja mengenai perencanaan, pengujian, dokumentasi, dan pengendalian perubahan. Dengan mengikuti standar tersebut, organisasi dapat memastikan bahwa sistem komputerisasi yang digunakan memenuhi persyaratan mutu, keamanan, dan kepatuhan regulatori [4]. Selain itu, validasi yang dilakukan secara sistematis dan berkelanjutan memastikan sistem tetap stabil, terkendali, dan mampu mendukung operasional farmasi secara efisien sepanjang daur hidupnya [5].
Penelitian ini menganalisis penerapan Computer System Validation (CSV) dengan meninjau faktor pendekatan berbasis risiko, kepatuhan regulasi, kualitas dokumentasi, manajemen perubahan, kompetensi personel, keterlibatan vendor, integritas data, serta pengelolaan siklus hidup sistem komputerisasi. Melalui penelitian ini, diharapkan dapat diperoleh pemahaman yang komprehensif mengenai peran CSV dalam menjamin integritas data, keandalan sistem, dan kepatuhan terhadap regulasi seperti CPOB Annex 7, FDA 21 CFR Part 11, dan pedoman EMA Edisi ke-2 tahun 2022. Validasi sistem komputer yang efektif tidak hanya memastikan bahwa sistem berjalan sesuai spesifikasi dan menghasilkan data yang akurat, tetapi juga berkontribusi pada peningkatan efisiensi proses, pengendalian risiko, serta penguatan sistem mutu secara keseluruhan. Dengan demikian, hasil penelitian ini diharapkan dapat menjadi dasar bagi optimalisasi kebijakan validasi sistem komputer di industri farmasi, serta mendukung pengembangan sistem digital yang lebih andal, aman, dan berkelanjutan.
Metode
Desain Studi
Penelitian ini merupakan Review Artikel yang dilakukan pada periode September hingga Oktober 2025. Fokus utama penelitian ini adalah melakukan kajian komprehensif terhadap penerapan Computerized System Validation (CSV) dalam industri farmasi. Penelaahan dilakukan terhadap berbagai sumber pustaka ilmiah, pedoman regulasi internasional, serta panduan teknis industri yang relevan, termasuk EU GMP Annex 11, FDA 21 CFR Part 11, serta pedoman GAMP 5 Edisi ke-2. Kajian ini mengintegrasikan aspek teoretis, regulatori, dan praktik terbaik (best practices) untuk memperoleh pemahaman yang menyeluruh mengenai peran CSV dalam menjamin mutu produk, kepatuhan terhadap regulasi, dan integritas data pada sistem komputerisasi di sektor farmasi, serta mengidentifikasi parameter kunci dan tantangan utama dalam penerapannya.[6].
Metode Analisis Study Literatur
Analisis dilakukan melalui penelaahan berbagai sumber pustaka, pedoman regulasi, dan dokumen pendukung yang relevan terkait penerapan Computerized System Validation (CSV) dalam industri farmasi. Sumber yang digunakan meliputi standar seperti Cara Pembuatan Obat yang Baik (CPOB) yang diterbitkan oleh BPOM, Good Manufacturing Practice (GMP), dan United States Pharmacopeia (USP). Kajian dilakukan dengan membandingkan prinsip, prosedur, serta ketentuan dalam setiap pedoman untuk menilai kesesuaian penerapan CSV terhadap regulasi yang berlaku secara nasional maupun internasional. Dengan mengaitkan hasil telaah dari berbagai literatur dan dokumen perusahaan, analisis ini memberikan gambaran menyeluruh mengenai tingkat kepatuhan dan relevansi praktik CSV di industri farmasi Indonesia terhadap standar mutu global [7].
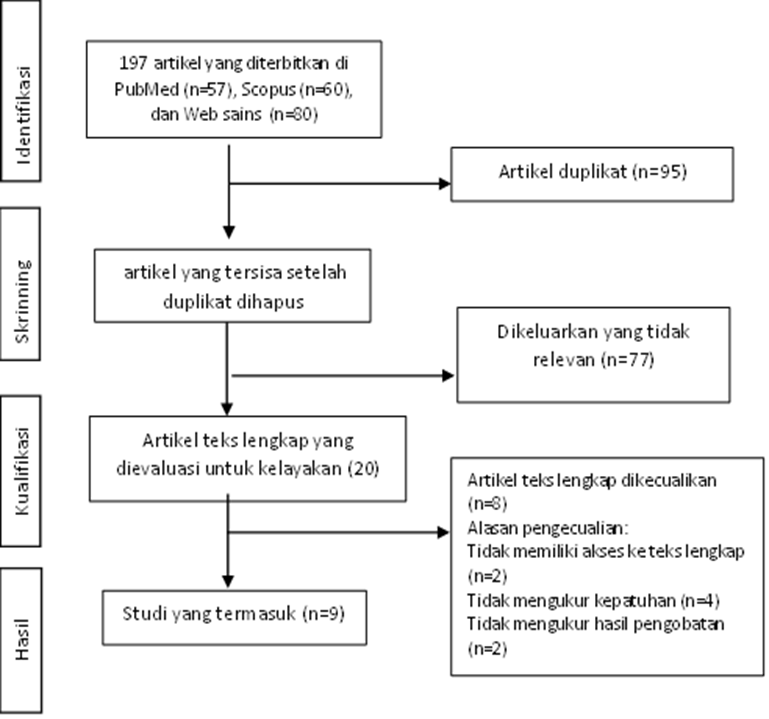
2.1 Alur Kajian periodik Sistem Komputerisasi di Industri Farmasi
Kajian periodik sistem komputerisasi dilakukan untuk memastikan validasi Computerized System Validation (CSV) tetap berlaku sesuai dengan ketentuan CPOB 2024, prinsip GMP, dan panduan USP <1058> tentang kualifikasi instrumen analitik. Kegiatan ini merupakan bagian dari manajemen siklus hidup sistem komputerisasi yang bertujuan memastikan sistem berfungsi sesuai tujuan, memenuhi persyaratan regulasi, serta menjaga integritas data sesuai prinsip ALCOA+ (Attributable, Legible, Contemporaneous, Original, Accurate, Complete, Consistent, Enduring, and Available) [8]. Validasi adalah proses sistematis yang bertujuan memastikan setiap kegiatan di fasilitas farmasi berjalan konsisten sesuai parameter yang telah ditetapkan. Melalui pengumpulan dan analisis data, validasi membuktikan bahwa suatu proses dapat menghasilkan keluaran yang stabil dan sesuai spesifikasi. Selain itu, validasi juga berperan dalam memastikan standar mutu dan kepatuhan terhadap regulasi terpenuhi secara berkelanjutan, serta bahwa fasilitas beroperasi sesuai pedoman current Good Manufacturing Practice (cGMP). Dengan demikian, validasi menjadi bukti terdokumentasi bahwa proses telah memenuhi kriteria yang ditetapkan dan dapat diandalkan untuk menghasilkan produk.
Hasil Penelitian
Tabel 1. Tabel Hasil Kajian Review
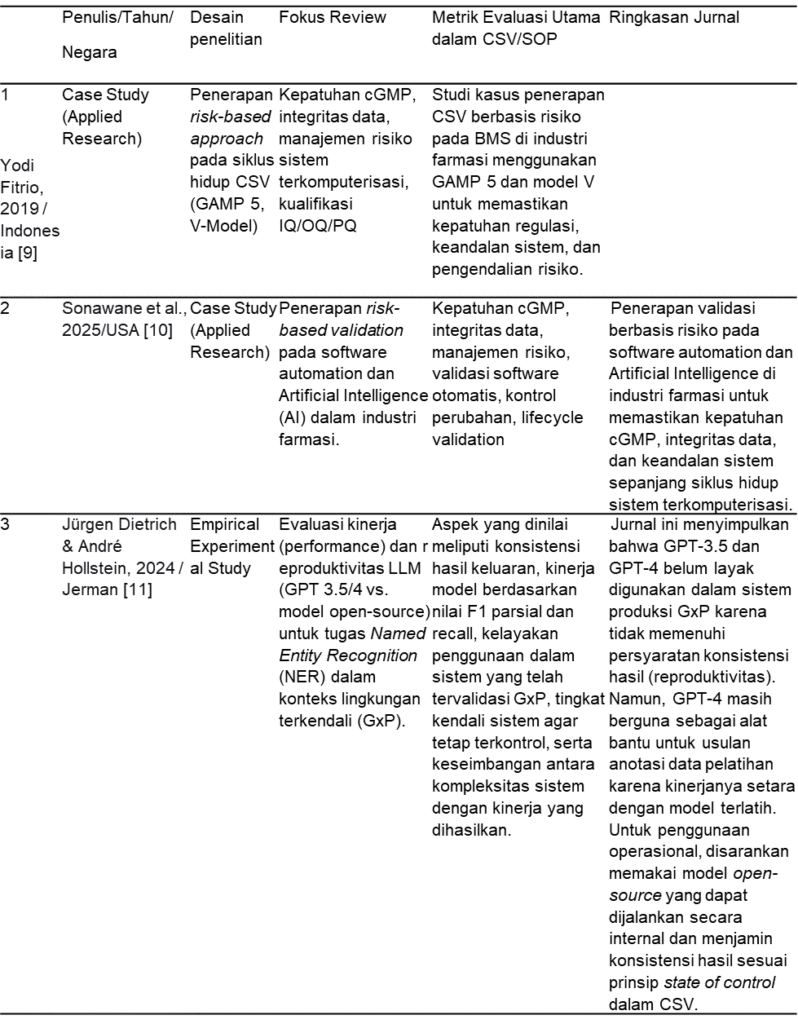

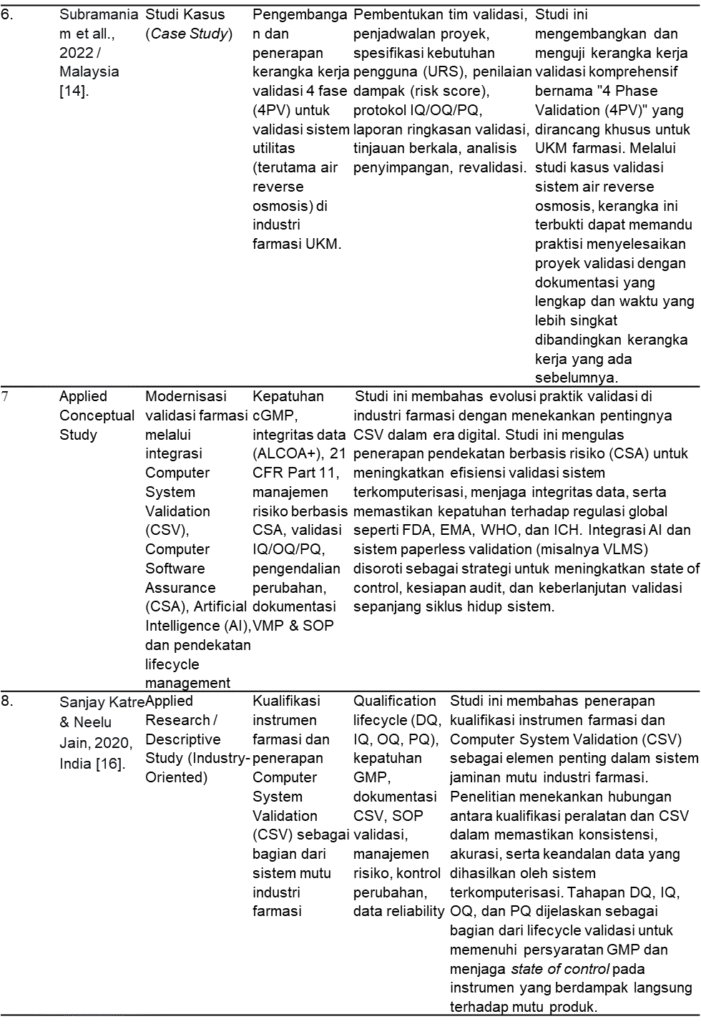

Pembahasan
Industri farmasi merupakan bidang yang memiliki standar dan ketentuan khusus yang wajib mengikuti pedoman Cara Pembuatan Obat yang Baik (CPOB). Dalam industri ini, kualitas menjadi aspek yang paling penting, sehingga penerapan sistem manajemen mutu dilakukan untuk memastikan obat yang dihasilkan memiliki mutu tinggi serta aman digunakan selama masa edarnya [18]. Mayoritas studi menunjukkan bahwa penerapan risk-based approach merupakan elemen fundamental dalam Computer System Validation (CSV) [9–11]. Tren utama yang mengemuka adalah pergeseran menuju risk-based approach, sebagaimana ditunjukkan dalam studi kasus oleh Fitrio [9] dan dikembangkan lebih lanjut oleh Sonawane et al. serta Kawarkhe et al.[10,11]. Pendekatan ini, yang mengadopsi kerangka kerja seperti GAMP 5, V-Model, dan Computer Software Assurance (CSA), memungkinkan alokasi sumber daya validasi yang lebih efisien dengan memfokuskan aktivitas pada area yang memiliki dampak tertinggi terhadap kualitas produk, integritas data, dan keselamatan pasien. Implementasi strategi ini tidak hanya memenuhi tuntutan regulasi yang ketat, seperti cGMP dan FDA 21 CFR Part 11, tetapi juga meningkatkan kelincahan dan keberlanjutan proses validasi sepanjang siklus hidup sistem [10,11].
Sistem komputerisasi memegang peranan esensial dalam operasional karena fungsinya untuk mengontrol, mendukung, dan mendokumentasikan proses. Mengingat fungsi kritis ini, tujuan fundamental dari implementasi sistem tersebut adalah untuk menjamin bahwa output informasi yang dihasilkan senantiasa akurat dan telah terverifikasi kesesuaiannya dengan spesifikasi yang telah ditetapkan [19]. Kajian ini menitikberatkan pada telaah literatur mengenai kesesuaian sistem komputerisasi dengan kerangka regulasi dan standar mutu terkini, termasuk ketentuan Cara Pembuatan Obat yang Baik (CPOB) 2024 [20]. Dalam industri farmasi, proses validasi dan kualifikasi menjadi langkah krusial yang diterapkan pada seluruh instrumen dan peralatan untuk memastikan setiap komponen beroperasi dengan benar dan konsisten dalam menjaga integritas produk. Sistem komputerisasi berperan penting dalam menjamin bahwa data dan informasi yang dihasilkan akurat serta sesuai dengan spesifikasi yang telah ditetapkan. Selain itu, sistem ini berfungsi untuk mengontrol, mendukung, dan mendokumentasikan berbagai proses yang berlangsung dalam kegiatan produksi dan pengawasan mutu [21].
Perkembangan teknologi informasi turut memperluas cakupan dan kompleksitas CSV, khususnya dengan meningkatnya penggunaan sistem canggih seperti Artificial Intelligence (AI) dan sistem pendukung keputusan otomatis [10,12]. Sonawane et al. 2025 mengkaji tantangan validasi perangkat lunak otomasi dan AI dalam konteks GxP, sementara pada penelitian yang dilakukan oleh Dietrich dan Hollstein. 2025 memberikan bukti empiris terkait keterbatasan Large Language Models (LLM) generatif, seperti GPT-4, yang dinilai belum memenuhi persyaratan reproduktibilitas dan determinisme yang kritis untuk digunakan secara langsung dalam lingkungan produksi GxP [10–12]. Oleh karena itu, mereka merekomendasikan penggunaan model open-source yang dapat dikendalikan secara internal guna menjamin keberlangsungan state of control. Sebaliknya, studi oleh Zapelini et al. 2022 dan Dahmke et al. 2024 menunjukkan bahwa sistem pendukung keputusan berbasis algoritma, seperti algoritma genetika, dapat divalidasi secara memadai untuk aplikasi klinis [12,13]. Sistem tersebut terbukti menghasilkan keluaran yang konsisten, akurat, dan sebanding dengan penilaian ahli, sehingga memperkuat peran CSV dalam meningkatkan keselamatan pasien dan mendukung pengambilan keputusan klinis yang andal.
Pondasi utama dari seluruh sistem tervalidasi tersebut adalah penerapan prinsip integritas data (ALCOA+), yang secara konsisten ditekankan dalam berbagai kajian [11,14]. Kawarkhe et al. 2025 serta Žagar dan Mihelič. 2022 menegaskan bahwa jaminan integritas data melalui kombinasi kontrol teknis dan prosedural yang memadai bukan hanya bertujuan untuk memenuhi kepatuhan regulasi, tetapi juga menjadi prasyarat bagi pemanfaatan data lanjutan, seperti analisis prediktif dan penerapan big data dalam kerangka Pharma 4.0. Selain itu, CSV tidak berdiri sendiri, melainkan terintegrasi erat dengan disiplin lain dalam sistem mutu farmasi. Katre dan Jain [8] menjelaskan bahwa kualifikasi peralatan (DQ, IQ, OQ, PQ) dan CSV merupakan dua aspek yang saling melengkapi dalam menjamin keandalan sistem terkomputerisasi secara menyeluruh, mencakup perangkat keras, perangkat lunak, dan proses operasional [15,17].
Sejalan dengan prinsip sistem mutu farmasi computer System Validation (CSV) tidak dapat dipisahkan dari penerapan sistem kualifikasi peralatan, yang meliputi tahapan Design Qualification (DQ), Installation Qualification (IQ), Operational Qualification (OQ), dan Performance Qualification (PQ). Pada tahap Design Qualification (DQ), dilakukan verifikasi terhadap pemenuhan User Requirements Specification (URS) sebagai dasar perancangan sistem, yang wajib diterapkan pada seluruh peralatan, sarana penunjang, dan sistem yang akan diadakan. Kualifikasi desain ini bertujuan untuk memastikan bahwa spesifikasi fungsional dan operasional instrumen telah didefinisikan secara memadai serta bahwa proses pengambilan keputusan, termasuk pemilihan pemasok, terdokumentasi dengan baik. Pelaksanaan DQ mencakup analisis kebutuhan dan permasalahan yang akan diselesaikan, penetapan tujuan penggunaan peralatan, identifikasi kondisi lingkungan operasional, evaluasi awal fungsi dan spesifikasi kinerja, proses seleksi pemasok secara bertahap hingga penetapan akhir, serta pengembangan dan dokumentasi spesifikasi fungsional dan operasional sebagai dasar pelaksanaan tahapan kualifikasi selanjutnya [22].
Installation Qualification (IQ) merupakan proses verifikasi terdokumentasi untuk memastikan bahwa peralatan atau sistem yang diinstal telah sesuai dengan spesifikasi yang tercantum dalam dokumen pemasangan serta dipasang mengikuti persyaratan teknis yang telah ditetapkan. Dalam konteks sistem terkomputerisasi, IQ mencakup verifikasi bahwa sistem komputer beserta seluruh perangkat lunak pendukungnya telah terinstal dengan benar, memenuhi standar teknik pabrikan, dan sesuai dengan spesifikasi yang disetujui [23]. Pelaksanaan IQ melibatkan peninjauan dan konfirmasi prosedur instalasi sebagaimana tercantum dalam installation guide, termasuk verifikasi konfigurasi perangkat keras dan perangkat lunak yang diinstal pada sistem yang ditentukan. Tantangan yang dapat muncul pada tahap ini antara lain ketidaksesuaian antara dokumentasi instalasi dengan kondisi instalasi aktual, yang berpotensi memengaruhi kesiapan sistem untuk melanjutkan ke tahap kualifikasi berikutnya [24].
Operational Qualification (OQ) merupakan tahapan pengujian kualifikasi yang dilaksanakan setelah Installation Qualification (IQ) dengan tujuan untuk memastikan dan mendokumentasikan bahwa sistem atau peralatan yang telah diinstal mampu beroperasi sesuai dengan spesifikasi yang telah ditetapkan [25]. Pelaksanaan OQ dilakukan berdasarkan protokol pengujian yang disusun sebelumnya, di mana seluruh fungsi kritis sistem diuji secara sistematis untuk memverifikasi kesesuaian kinerja operasionalnya. Berdasarkan hasil pengujian tersebut, dilakukan analisis data guna menarik kesimpulan terkait kemampuan sistem dalam memenuhi persyaratan operasional yang ditentukan [26]. Dalam konteks sistem terkomputerisasi, OQ mencakup verifikasi fungsi sistem sekaligus konfirmasi keabsahan hasil Installation Qualification, termasuk pengujian bahwa perangkat lunak, seperti Chromeleon, beroperasi sesuai dengan spesifikasi dalam lingkungan kerja yang ditetapkan. Selain itu, OQ memastikan bahwa pengujian tidak dilakukan saat terdapat proses aktif, karena sistem akan secara otomatis membatalkan pengujian dan menampilkan pesan peringatan, yang menunjukkan mekanisme pengendalian operasional telah berfungsi dengan baik [27].
Performance Qualification (PQ) dilaksanakan setelah penyelesaian Installation Qualification (IQ) dan Operational Qualification (OQ), dengan tujuan untuk memverifikasi dan mendokumentasikan bahwa sistem atau peralatan mampu memenuhi persyaratan kinerja yang telah ditetapkan serta secara konsisten menghasilkan keluaran yang sesuai dengan spesifikasi dalam kondisi penggunaan rutin. Pelaksanaan PQ dilakukan berdasarkan protokol yang telah disusun sebelumnya dan berfokus pada pengujian parameter-parameter kritis, termasuk pengendalian tingkat akses pengguna (access level) dan fungsi audit trail [28]. Pengujian tingkat akses bertujuan untuk memastikan bahwa sistem yang dioperasikan telah menerapkan kebijakan dan prosedur otorisasi sesuai dengan peran atau roles yang didefinisikan.
Pada perangkat lunak Chromeleon, misalnya, terdapat dua peran utama, yaitu analis dan administrator, yang masing-masing memiliki kewenangan berbeda. Dalam pengujian ini, dilakukan simulasi berbagai skenario penggunaan untuk memverifikasi bahwa setiap peran hanya dapat melakukan fungsi sesuai dengan otoritas yang dimilikinya [29]. Hasil pengujian menunjukkan bahwa sejumlah fungsi administratif, seperti menyalin atau menghapus folder, mengubah status folder menjadi read-only, serta mengakses laporan dan tanda tangan elektronik, tidak dapat dilakukan oleh peran analis. Pembatasan akses terhadap laporan dan tanda tangan elektronik yang merupakan data elektronik terenkripsi atau yang secara langsung terkait dengan dokumen elektronik diterapkan untuk menjamin integritas data dan informasi yang telah ditandatangani, sehingga mendukung pemeliharaan sistem mutu dalam industri farmasi.
Tantangan implementasi Computer System Validation (CSV) pada organisasi dengan keterbatasan sumber daya khususnya usaha kecil dan menengah (UKM) di sektor farmasi telah menjadi perhatian penting dalam literatur terkini. Subramaniam et al. mengusulkan kerangka kerja 4 Phase Validation (4PV) sebagai pendekatan yang disederhanakan namun tetap selaras dengan prinsip-prinsip regulatori GxP [14]. Kerangka ini menekankan penyelarasan aktivitas validasi dengan tingkat risiko dan kompleksitas sistem, sehingga memungkinkan penerapan CSV yang lebih proporsional tanpa menghilangkan elemen kritis seperti dokumentasi, pengujian fungsional, dan pengendalian perubahan. Temuan ini memperkuat pandangan bahwa kepatuhan regulasi tidak selalu identik dengan kompleksitas berlebihan, melainkan dapat dicapai melalui pendekatan metodologis yang adaptif dan kontekstual sesuai dengan kapasitas organisasi.
Secara lebih luas, literatur yang dianalisis menunjukkan bahwa CSV telah berevolusi menjadi strategi manajemen mutu dan risiko yang proaktif, melampaui perannya sebagai sekadar daftar periksa kepatuhan. Fokus CSV kini diarahkan pada pencapaian dan pemeliharaan state of control yang berkelanjutan, yaitu kondisi di mana sistem terkomputerisasi beroperasi secara konsisten, andal, dan terkendali sepanjang siklus hidupnya. Pendekatan ini menempatkan CSV sebagai bagian integral dari tata kelola sistem mutu, yang mendukung pengambilan keputusan berbasis data, ketahanan proses, serta kesiapan organisasi dalam menghadapi audit dan perubahan teknologi. Dengan demikian, CSV berkontribusi langsung terhadap keberlangsungan operasional dan perlindungan kualitas produk dalam lingkungan industri yang semakin kompleks dan terdigitalisasi.
Pendekatan ini menunjukkan bahwa prinsip-prinsip CSV yang ketat tetap dapat diterapkan secara efektif melalui adaptasi metodologis yang proporsional, tanpa mengorbankan kepatuhan regulasi maupun kelayakan operasional. Secara keseluruhan, literatur yang dianalisis menggambarkan CSV sebagai strategi manajemen risiko dan mutu yang proaktif serta terus berevolusi, melampaui fungsi tradisionalnya sebagai daftar periksa kepatuhan. Perkembangan inovatif dalam pendekatan Computer Software Assurance (CSA), penerapan otomasi validasi melalui konsep paperless validation dan Validation Lifecycle Management System (VLMS), serta pemanfaatan data real-time untuk pemantauan berkelanjutan dipandang sebagai elemen kunci dalam meningkatkan efektivitas dan keberlanjutan proses CSV. Melalui integrasi yang selaras antara prinsip berbasis risiko, teknologi digital, dan kerangka kerja sistem mutu yang kuat, CSV diharapkan tetap berperan sebagai pilar strategis dalam menjamin keamanan produk, mendorong kemajuan inovasi terapetik, serta mendukung transformasi digital industri farmasi secara berkesinambungan [30].
Fokus CSV kini diarahkan pada pencapaian dan pemeliharaan state of control yang berkelanjutan, yaitu kondisi di mana sistem beroperasi secara konsisten, andal, dan terkendali sepanjang siklus hidupnya. Tantangan di masa depan diperkirakan akan semakin berpusat pada validasi sistem yang otonom dan adaptif, seperti AI, sambil tetap mempertahankan fondasi integritas data dan kepatuhan regulasi. Inovasi dalam pendekatan CSA, otomasi validasi (paperless validation, Validation Lifecycle Management System), serta pemanfaatan data real-time untuk pemantauan berkelanjutan akan menjadi faktor kunci dalam menjaga relevansi CSV sebagai pilar utama dalam mendukung keamanan produk, inovasi terapetik, dan transformasi digital industri farmasi [9–11].
Kesimpulan
Computer System Validation (CSV) merupakan komponen esensial dalam sistem manajemen mutu industri farmasi yang berfungsi menjamin keandalan sistem terkomputerisasi, integritas data, dan kepatuhan regulasi. Penerapan pendekatan berbasis risiko, yang terintegrasi dengan tahapan kualifikasi peralatan (DQ, IQ, OQ, dan PQ), terbukti efektif dalam menjaga state of control sepanjang siklus hidup sistem, sekaligus meningkatkan efisiensi proses validasi.
Seiring dengan perkembangan teknologi digital, pendekatan CSV dituntut semakin adaptif tanpa mengabaikan prinsip dasar mutu dan integritas data. Inovasi seperti Computer Software Assurance (CSA), paperless validation, dan Validation Lifecycle Management System (VLMS) memberikan peluang untuk memperkuat efektivitas dan keberlanjutan CSV, termasuk pada organisasi dengan sumber daya terbatas, sehingga CSV tetap relevan sebagai pilar strategis dalam mendukung keamanan produk dan transformasi digital industri farmasi.
Daftar Pustaka
1. BPOM RI. Peraturan Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 7 Tahun 2024 tentang Standar Cara Pembuatan Obat yang Baik. Jakarta: KEMENKES; 2024.
2. Meenal KD. Benefits Of Computer System Validation In Pharmaceutical Industry. International Journal Of Pharceutical Sciences 2024;2:1012–9.
3. Giacobbe DR, Mora S, Signori A, Russo C, Brucci G, Campi C, et al. Validation of an Automated System for the Extraction of a Wide Dataset for Clinical Studies Aimed at Improving the Early Diagnosis of Candidemia. Diagnostics 2023;13:961. https://doi.org/10.3390/diagnostics13050961.
4. International Society Pharmaceutical Engineering. A Risk-Based Approach to Compliant GxP Computerized Systems (Second Edition). International Society for Pharmaceutical Engineering; 2022.
5. Ain NK. Importance of Qualification, Computer System Validation and its Regulatory Compliance in Pharmaceutical Industry. International Journal of Drug Regulatory Affairs 2020;8:70–7.
6. Savitha S dan Katherisan K. Computerized System Validation – A Review. Int J Biol Pharm Allied Sci 2022;11. https://doi.org/10.31032/IJBPAS/2022/11.11.6567.
7. Raja JR, Kella A, Narayanasamy D. The Essential Guide to Computer System Validation in the Pharmaceutical Industry. Cureus 2024. https://doi.org/10.7759/cureus.67555.
8. Rajveer Bhaskar. Review on :- Computer System Validation In Pharma Industry. International Journal of Pharmaceutical Research and Applications 2023;8.
9. Fitrio Y. Case Study Risk Based Approach for Life Cycle Computerized System in Pharmaceutical Industry. Journal of Applied Information, Communication and Technology 2019;6:61–73. https://doi.org/10.33555/ejaict.v6i2.66.
10. Sonawane SS, Baviskar MD. Risk- Based Validation of Software, Automation and Artificial intelligence in Pharmaceuticals. Biosci Biotechnol Res Asia 2025;4:1279. https://doi.org/10.13005/bbra/3441.
11. Dietrich J, Hollstein A. Performance and Reproducibility of Large Language Models in Named Entity Recognition: Considerations for the Use in Controlled Environments. Drug Saf 2025;48:287–303. https://doi.org/10.1007/s40264-024-01499-1.
12. Zapelini CM, Galato D, Alano GM, de Carvalho Martins KS, Trauthman SC, Soares A, et al. Validation of a computerized decision support system to review pharmacotherapy treatment: scheduling guidelines. BMC Med Inform Decis Mak 2022;22:172. https://doi.org/10.1186/s12911-022-01914-6.
13. Dahmke H, Cabrera-Diaz F, Heizmann M, Stoop S, Schuetz P, Fiumefreddo R, et al. Development and validation of a clinical decision support system to prevent anticoagulant duplications. Int J Med Inform 2024;187:105446. https://doi.org/10.1016/j.ijmedinf.2024.105446.
14. Subramaniam VS, Prakash J, Kamaruddin S, Khoo SW. A comprehensive validation framework addressing utility parameter validation for application in small and medium enterprises (SMEs):A case study in pharmaceutical industry. Cogent Eng 2023;10. https://doi.org/10.1080/23311916.2023.2166219.
15. Kawarkhe S. Modernizing Pharmaceutical Validation: Integrating CSA, AI, AND Lifecycle Management Principles. Scientific Research Journal of Medical and Health Science 2025;3.
16. Katre S, Jain N. Qualification And Computer System Validation Of Pharmaceutical Instrument: Critical Quality Attributes In Pharmaceutical Industry. Int J Pharm Sci Res 2020;11:5182. https://doi.org/10.13040/IJPSR.0975-8232.11(10).5182-91.
17. Žagar J, Mihelič J. Big data collection in pharmaceutical manufacturing and its use for product quality predictions. Sci Data 2022;9:99. https://doi.org/10.1038/s41597-022-01203-x.
18. Raja JR. The Essential Guide to Computer System. Cureus 2024;16.
19. Katre SJ. Qualification and computer system validation of pharmaceutical instrument: critical quality attributes in pharmaceutical industry. J Pharm Sci, 2020;11.
20. BPOM. Badan Pengawasan Obat Dan Makanan Peraturan Kepala Badan Pengawas Obat Dan Makanan Republik Indonesia Nomor HK.00.05.41.1381 Tentang Tatalaksana Pendaftaran Suplemen Makanan Dengan Rahmat Tuhan Yang Maha Esa Kepala Badan Pengawas Obat Dan Makanan Republik Indonesia. n.d.
21. Dewi NP. Farmasi Industri. Bandung: MediaSainsIndonesia; 2020.
22. Kezia V Krisanti, Ahmad S Abdulah, Dani Nugraha. Review: Kualifikasi Peralatan Dan Mesin Di Industri Farmasi. Farmaka 2022;20:27–35.
23. Avinasha S, Gangadharappa H V, Hemanth Kumar S, Gowrav M P. A Review on qualification of the tablet compression machine. International Journal of Research in Pharmaceutical Sciences 2020;11:1961–7. https://doi.org/10.26452/ijrps.v11i2.2124.
24. Rahmah R, R.H.P F, Wathoni N. Kualifikasi Sistem Komputerisasi Perangkat Lunak pada UHPLC di Salah Satu Industri Farmasi. Majalah Farmasetika 2025;10:144–58. https://doi.org/10.24198/mfarmasetika.v10i2.62299.
25. Dewi N.P., Pratiwi P.D., Deniyati, Sibadu M.S., Hadiq S, Kusumawati.D.E. Farmasi Industri. Bandung: Media Sains Indonesia; 2020.
26. Singh Asheesh SP. Computer system validation in the perspective of the pharmaceutical industry. Journal of Drug Delivery & Therapeutics 2018;8.
27. Patil Yogesh, Mali Kamlesh, Bodhane Mohini, Lale Shivam, Ram Phad, Shaikh Ismail. Computer System Validation:A Review. World J Pharm Res 2017;4:444–54.
28. Kiva Agita, Patihul Husni. Kualifikasi Kinerja Sistem Tata Udara Ruang Timbang Kelas E Di Industri Farmasi X. Farmaka 2023;22.
29. Parmal G. Review On:-Computerized System Validation: Process, Methods and its Implications. International Journal of Pharmaceutical Research and Applications 2023;8:485. https://doi.org/10.35629/7781-0805485494.
30. Simonovski N, Gjorgjeska B. Benefits from paperless computer system validation in pharmaceutical industry. Macedonian Pharmaceutical Bulletin 2022;68:123–4. https://doi.org/10.33320/maced.pharm.bull.2022.68.03.057.
cara mengutip artikel
https://jurnal.unpad.ac.id/farmasetika/rt/captureCite/69580/27337
 Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3
Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3