Majalah Farmasetika, 8 (2) 2023, 175-193
https://doi.org/10.24198/mfarmasetika.v8i2.41779
Artikel Penelitian
1Haflin, 2Agusriani, 3Ruri Putri Mariska, 4Ifti Sarah Zulfani , 5Barmi Hartesi*
1,2Program Studi Farmasi Poltekkes Kemenkes Jambi
3,4,5 Program Studi Farmasi, STIKES Harapan Ibu, Jambi, Indonesia
*E-mail: barmi.hartesi@gmail.com
(Submit 07/12/2022, Revisi 11/01/2023, Diterima 18/01/2023, Terbit 23/01/2023)
Abstrak
Penggunaan polimer pada sediaan sabun kertas sangat mempengaruhi bentuk sediaan dikarenakan sifat polimer memiliki volume rasio yang kecil sehingga sediaan yang dihasilkan menjadi elastis dan ringan. Polimer yang akan digunakan oleh peneliti yaitu polimer HPMC (Hydroxylpropyl methyl cellulose) dan PVA (Polivinil alcohol) dikarenakan polimer HPMC bersifat netral dan stabil dalam berbagai pH serta sediaan yang dihasilkan akan tampak jernih dan dapat membentuk film dengan baik [1] sedangkan polimer PVA dapat memudahkan difusi sediaan karena dapat terikat dengan air sehingga mudah diproses dalam pembuatan sediaan [2] maka hal tersebut menjadi pemicu bagi peneliti untuk melakukan uji pengaruh penggunaan polimer HPMC dan PVA terhadap kualitas sediaan sabun kertas dengan menggunakan zat aktif ekstrak metanol daun sungkai (Peronema canescens Jack) yang digunakan sebagai antibakteri. Penelitian ini bertujuan mengetahui pengaruh polimer HPMC dan PVA pada sediaan sabun kertas ekstrak metanol daun sungkai dan mengetahui aktivitas antibakteri sediaan sabun kertas ekstrak metanol daun sungkai menggunakan polimer yang berbeda. Formula sediaan diperoleh dari ekstraksi metanol daun sungkai dalam sediaan sabun kertas pencuci tangan antibakteri terhadap bakteri Staphylococcus aureus. Metode pengujian antibakteri menggunakan difusi cakram. Hasil penelitian menunjukkan sediaan yang baik yaitu pada sediaan F2B dengan formula sebagai berikut : Ekstrak daun sungkai (1%), HPMC (0,75%), Gliserin (1,25%), NaOH 50% (2,5%), Sodium lauryl sulfate (1,25%), Disodium EDTA (0.05%), Aquadestilata (ad 25) setiap masing-masing evaluasi seperti oganoleptis dengan hasil bentuk tipis elastis berbau khas sungkai dan berwarna hijau pekat, uji pH dengan hasil yang didapatkan yaitu 7,1, uji kestabilan busa dengan hasil yang didapatkan yaitu 94,2%, uji kadar asam lemak dan alkali bebas dengan hasil yang didapatkan yaitu 0,06%, dan uji kadar air mendapatkan hasil 15%. semua uji yang dilakukan telah memenuhi persyaratan uji menurut SNI. Hasil uji aktivitas antibakteri sabun kertas ekstrak metanol daun sungkai dengan konsentrasi 1% serta konsentrasi polimer HPMC 0,75% dapat menghambat bakteri Staphylococcus aureus dengan kategori zona hambat yang sedang yaitu persentase sebesar 5-10 mm.
Kata kunci: P. Canescens Jack, Polimer, Sabun Kertas, S. aureus.
Teks Lengkap:
Pendahuluan
Sungkai (Paronema canescens Jack) merupakan tumbuhan liar yang bernilai ekonomis, banyak masyarakat yang membudidayakannya, secara alami sungkai terdapat di Pulau Kalimantan, Sumatera, Kepulauan Riau, dan Jawa Barat. Bagian daun sungkai mengandung metabolit sekunder seperti alkaloid, flavonoid, dan tannin [3]. Tumbuhan sungkai dapat dijumpai di hutan, kebun, maupun halaman. Sungkai dapat tumbuh dengan mudah dan tidak perlu perawatan khusus, sehingga tanaman ini juga digunakan sebagai pembatas atau pagar hidup pekarangan rumah [4]. Secara empiris, daun sungkai dimanfaatkan oleh sebagian masyarakat untuk sakit gigi dan penurun demam [5]. Selain itu, daun sungkai juga bisa digunakan sebagai antibakteri, untuk nilai KHM ekstrak daun sungkai untuk bakteri S.mutans, S.thiposa, dan S.aureus adalah konsentrasi 20%, sedangkan untuk bakteri B.subtilis sebesar 15% dan untuk nilai KBM ekstrak daun sungkai pada konsentrasi 5% efektif membunuh bakteri S.mutans dan S.thiposa, sedangkan konsentrasi 1% efektif membunuh bakteri B.subtilis dan S.aureus
Sediaan yang dapat dijadikan sebagai antibakteri dikenal sebagai antiseptik. Antiseptik adalah senyawa kimia yang digunakan untuk menghambat atau mematikan mikroorganisme pada jaringan hidup, yang mempunyai efek membatasi dan mencegah infeksi agar tidak menjadi parah. Sediaan antiseptik yang dibuat menggunakan zat aktif ekstrak tumbuhan di ekstraksi menggunakan pelarut, salah satu contohnya yaitu pelarut etanol dan metanol [6]. Pelarut metanol lebih unggul digunakan dalam proses pembuatan sediaan antibakteri menggunakan zat aktif ekstrak tumbuhan dikarenakan pelarut metanol lebih mudah menarik senyawa metabolit sekunder yang terkandung dalam tumbuhan sampel selain itu juga ekstrak tumbuhan yang menggunakan pelarut metanol untuk daya hambat aktifitas antibakteri lebih besar dibandingkan dengan pelarut etanol [6]. Menurut [7] menyatakan bahwa ekstrak daun sungkai yang menggunakan pelarut metanol memiliki spektrum penghambatan antibakteri pada bakteri Staphylococcus aureus dengan konsentasi terkecil yaitu 5% – 20% dengan daya hambat sebesar 6,13 mm – 7,66 mm yang termasuk dalam daya hambat katageori sedang. Bentuk sediaan antiseptik yang beredar dipasaran salah satunya yaitu sabun [8].
Sediaan sabun antiseptik yang beredar di masyarakat antara lain sabun padat, sabun cair dan sabun transparan (Habibah et al., 2017). Selain itu, ada salah satu sabun yang saat ini sedang trend di masyarakat yaitu sabun kertas. Keunggulan sabun kertas adalah praktis, ringan, mudah dibawa kemana-mana, higienis dalam penyimpanannnya serta ramah lingkungan. Sabun kertas merupakan bentuk lembaran, ukuran kecil dan tipis sehingga mudah dibawa dan cocok untuk digunakan diperjalanan jauh atau keluar rumah. Pembuatan sabun kertas ini sendiri sama seperti sabun pada umumnya hanya saja untuk pembuatan sabun kertas terbuat dari antara polimer yang larut air dan sabun [9].
Polimer dalam bidang farmasi terbagi menjadi dua yaitu polimer sintetik dan polimer alam. Polimer sintetis adalah polimer yang dibuat dari molekul sederhana (monomer) dalam pabrik atau polimer yang dibuat dari bahan baku kimia disebut polimer sintetis seperti polyetana, polipropilena, polyvinil chlorida (PVC), polyvinil alcohol (PVA), dan nylon. Polimer sintetik yang digunakan dalam penelitian ini adalah PVA (Polyvinil alcohol) dimana polimer ini dapat memudahkan difusi sediaan karena dapat terikat dengan air sehingga mudah diproses dalam pembuatan sediaan [2].
Polimer semi sintetis (alam) adalah senyawa yang dihasilkan dari proses metabolisme makhluk hidup. Jumlahnya yang terbatas dan sifat polimer alam ini kurang stabil, mudah menyerap air dan sukar dibentuk menyebabkan penggunaannya amat terbatas. Contoh polimer semi sintetis adalah metil selulosa, etil selulosa, HPMC (Hydroxylpropyl methyl cellulose), hidroksil propil selulosa, hidroksil etil selulosa dan hidroksil etil metil selulosa. Polimer semi sintetik yang digunakan pada penelitian ini adalah HPMC (Hydroxylpropyl methyl cellulose) yang bersifat netral dan stabil dalam berbagai pH sehingga dapat memperpanjang penyimpanan dalam waktu yang lama. Kelebihan dari polimer ini yaitu sediaan jernih, tidak mengiritasi kulit, bersifat non toxic dan membentuk film dengan baik serta tahan pada kelembapan [1]. Dari uraian diatas, maka peneliti tertarik untuk melakukan penelitian mengenai pengaruh penggunaan polimer terhadap kualitas sabun kertas menggunakan zat aktif ekstrak metanol daun sungkai (Peronema canescens Jack) sebagai antibakteri
Metode
Alat
Alat yang digunakan pada penelitian ini adalah timbangan analitik (Ohaus®), vaccum rotary evaporator (Buchi®), autoclave (Hirayama®), laminar air flow (Kojair®), homogenizer, vortex (Thermo®), magnetic stirrer, kertas saring, pH meter(Hanna®), kertas cakram, inkubator, jarum ose, pinset, lemari pendingin (LG®), waterbath (6 Hole Electric®), Kuas, objek glass, cover glass, spatula dan alat – alat gelas yang terdapat pada laboratorium.
Bahan
Bahan yang digunakan pada penelitian ini adalah Daun sungkai (Peronema canescens Jack), Metanol, Aqua destilata, HPMC, PVA (Sigma®), Gliserin, NaOH 30%, Sodium lauril sulfat (Making Cosmetics®), Disodium EDTA, Soluble water paper, Bakteri Staphylococcus aureus, Mueller-Hinton agar (Merck®), Mueller-Hinton broth (Himedia®), sampel sabun kertas yang beredar dipasaran.
Prosedur Rinci
- Sampel daun sungkai (Peronema canescens Jack) diperoleh dari daerah Muara Kilis, Kabupaten Tebo, Provinsi Jambi.
- Determinasi tanaman dilakukan di Laboratorium Taksonomi Tumbuhan Jurusan Biologi FMIPA UNPAD
- Sampel tumbuhan dicuci dan dirajang, keringkan pada tempat yang tidak terkena sinar matahari langsung selama 3-5 hari, selanjutnya daun dihaluskan sehingga diperoleh serbuk daun sungkai. Proses ekstraksi dilakukan dilakukan dengan metode maserasi menggunakan pelarut metanol 95%. Ekstrak cair yang diperoleh kemudian dipekatkan menggunakan Rotary vaccum evopator.
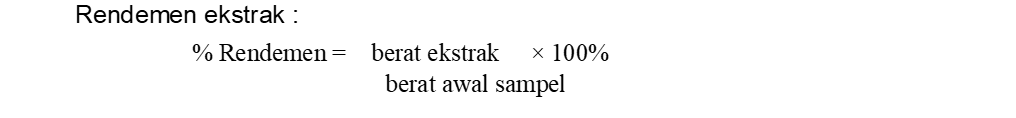
4. Skrining fitokimia terdiri dari uji alkaloid, flavonoid, saponin, tanin dan steroid. Pengujian ini dilakukan untuk mengidentifikasi senyawa metabolit sekunder yang terdapat pada sampel.
a. Uji alkaloid
Uji alkaloid dilakukan dengan cara menimbang sampel ekstrak 0,5 gram dimasukan kedalam tabung reaksi, tambahkan 2 mL kloroform dan 2 mL amonia. Kemudian disaring dan tambahkan 3 – 5 tetes H₂SO₄. Hasil dikocok dan biarkan membentuk 2 lapisan, kemudian filtrat dibagi menjadi 3 bagian dan dilakukan pengujian menggunakan beberapa tetes pereaksi Mayer, Dragondrof, dan Wagner. Larutan pada perekasi Mayer terdapat endapan putih menandakan hasil positif, larutan pada perekasi Dragondrof terdapat perubahan warna menjadi merah jingga menandakan hasil positif dan larutan pada pereaksi Wagner menghasilkan endapan coklat menandakan hasil positif [10].
b. Uji flavonoid
Uji flavonoid dilakukan dengan cara menimbang 1 gram sampel ekstrak lalu dimasukan kedalam tabung reaksi setelah itu ditambahkan 5 mL aquadest lalu dikocok dan dipanaskan lalu dikocok lagi kemudian disaring. Selanjutnya ditambahkan Mg 0,2 gram dan 3 tetes HCl. Terbentuknya warna merah/jingga pada larutan menunjukan adanya flavonoid [10].
c. Uji saponin
Uji saponin dilakukan dengan cara menimbang 0,5 gram lalu dimasukan kedalam tabung reaksi dan ditambahkan 5 mL aquadestilata yang dipanaskan kemudian ditambahkan 2 tetes HCl 1N. Hasil sampel terbentuknya buih maka ekstrak positif mengandung saponin [10].
d. Uji tanin
Uji tanin dilakukan dengan cara menimbang 0,5 gram lalu dimasukan kedalam tabung reaksi dan dilarutkan dengan 10 mL aquadestilata, kemudian disaring menggunakan kertas saring. Selanjutnya filtrat yang diperoleh diambil sebanyak 2 mL kemudia ditambahkan 2 tetes pereaksi FeCl₃ 1%. Jika terbentuk warna biru atau hijau kehitaman menunjukan adanya tanin [10].
e. Uji steroid
Diambil sampel sebanyak 1 gram lalu ditambahkan 20 mL kloroform dan diletakan didalam tabung reaksi yang kering, kemudian tambahkan pereaksi liebermann burchard (asam asetat anhindrat dan asam sulfat pekat). Reaksi positif akan ditunjukan dengan adanya warna hijau kebiruan [10].
5. Formula Sediaan
Tabel 1 Formula Sediaan

polimer HPMC 0,5%
F2A : Formula dengan menggunakan konsentrasi ekstrak 0% dan polimer HPMC 0,75%
F2B : Formula dengan menggunakan konsentrasi ekstrak 1% dan polimer HPMC 0,75%
F3A : Formula dengan menggunakan konsentrasi ekstrak 0% dan polimer PVA 1,75%
F3B : Formula dengan menggunakan konsentrasi ekstrak 1% dan polimer PVA 1,75%
F4A : Formula dengan menggunakan konsentrasi ekstrak 0% dengan polimer PVA 2%
F4B : Formula dengan menggunakan konsentrasi ekstrak 1% dengan polimer PVA 2%
Proses pembuatan dilakukan menggunakan metode panas dengan waterbath. Dimana polimer HPMC/PVA dimasukan kedalam beaker glass dan dikembangkan terlebih dahulu menggunakan aquadestilata panas dengan pengadukan konstan menggunakan homogenizer hingga mengembang. Kemudian masukan NaOH 50% dan ekstrak metanol daun sungkai. Kemudian tambahkan bahan pendukung lainnya yaitu : Gliserin, SLS, Dinatrium EDTA dan ad 25 mL aquadest, kemudian aduk secara konstan menggunakan homogenizer lalu dinginkan dan oleskan larutan diatas soluble water paper dan dikeringkan kemudian dilanjutkan evaluasi sediaan seperti :
a. Uji Stabilitas
Sabun disimpan disuhu 25°C dan 40°C selama 28 hari, lihat perubahannya [11].
b. Uji Kadar Air
2 gram sabun yang sudah dihaluskan dimasukkan kedalam cawan petri, lalu masukkkan kedalam oven pada suhu 105°C selama 1 jam [12].
c. Uji Asam Lemak dan Kadar Alkali Bebas
5 gram sabun dimasukkan kedalam alkohol netral dan dipanaskan pada suhu 100°C dan didihkan selama 30 menit, lalu amati [13].
d. Uji Tinggi Busa dan Stabilitas Busa
1 gram sabun dimasukkan kedalam tabung reaksi yang berisi 10mL aquadest, homogenkan dengan cara membolak-balikan tabung selama 5 menit, lalu amati [14].
7. Uji Aktivitas Antibakteri
Uji ini digunakan 6 cawan yang telah berisi media MHA dengan kontrol (+) sabun kertas yang beredar dipasaran, kontrol (-) basis sabun kertas tanpa ekstrak daun sungkai dan konsentrasi sabun kertas ekstrak daun sungkai masing-masing formula [15].
Hasil
Skrining Fitokimia
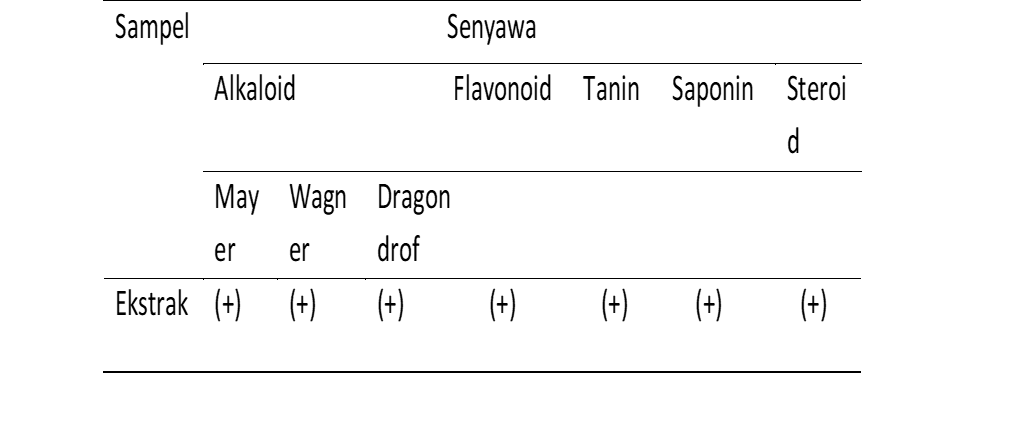
Pada penelitian ini menggunakan tumbuhan sungkai, dimana tumbuhan sungkai memiliki berbagai manfaat salah satunya sebagai antibakteri [3]. sebelum dilakukan pengujian, tumbuhan sungkai dilakukan skrining fitokimia terlebih dahulu yang mana pengujian fitokimia ini meliputi : alkaloid, flavonoid, saponin, tanin dan steroid. Dari hasil yang didapatkan ekstrak metanol daun sungkai mengandung metabolit sekunder dengan hasil skrining fitokimia positif.
Tabel 2 Hasil Skrining Fitokimia
Uji Organoleptis
Sabun kertas pencuci tangan selanjutnya dilakukan uji evaluasi. Hasil uji organoleptis yang didapatkan pada F1A, F2A, F3A, dan F4A (basis) berwarna putih tulang, berbau khas sedikit tajam, untuk sediaan F1A dan F2A memiliki tekstur yang tipis dan elastis sedangkan pada sediaan F3A dan F4A memiliki tekstur sediaan yang tipis dan kaku, dan untuk sediaan formulasi sabun yang mengandung ekstrak metanol daun sungkai pada F1B, F2B, F3B dan F4B memiliki bau khas sungkai, untuk sediaan F1B dan F3B memiliki warna hijau yang lebih muda dibandingkan dengan F2B dan F4B.

Pengujian pH
Pengujian pH dilakukan pada sediaan yang bertujuan untuk melihat tingkat keasaman sediaan sehingga menjamin sediaan tidak menyebabkan iritasi pada kulit(10). Hasil rata-rata uji pH pada sediaan sabun kertas F1A, F1B, F2A, F2B, F3A, F3B, F4A dan F4B didapatkan nilai pH berturut-turut yaitu 7,3 ± 0,5, 7,8 ± 0,3, 7,2 ± 0,1, 7,1 ± 0,2, 7,6 ± 0,1, 7,3 ± 0,1, 7,7 ± 0,1, 7,1 ± 0,1. Parameter untuk nilai pH pada sabun pencuci tangan menurut SNI 06-4085-1996 adalah 6 – 8, sehingga dari keseluruhan formula sudah memenuhi parameter pH yang baik sebagai sediaan sabun pencuci tangan.
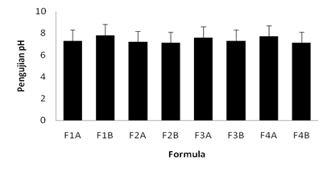
Gambar 2. Hasil Uji pH
Uji Kestabilan Busa
Hasil uji tinggi dan kestabilan busa pada sediaan sabun kertas pencuci tangan memiliki hasil pada F1A sebesar 89,4% ± 0,55, pada F1B memiliki hasil sebesar 94,9% ± 1,76, pada F2A memiliki hasil sebesar 93,9% ± 2,38, pada F2B memiliki hasil sebesar 94,2% ± 2,39, pada F3A memiliki hasil sebesar 93,0% ± 1,41, pada F3B memiliki hasil sebesar 93,8% ± 0,2, pada F4A memiliki hasil sebesar 94,6% ± 1,17 dan pada F4B memiliki hasil sebesar 93,8% ± 2,34. Dari hasil tersebut menunjukan bahwasannya nilai stabilitas busa yang berbeda-beda setiap perlakuan. Parameter untuk nilai uji kestabilan busa pada sabun pencuci tangan menurut SNI 06-4085-1996 adalah 60%-70% sehingga keseluruhan formula memenuhi persyaratan paramater SNI yang baik.

Pengujian Kadar Air
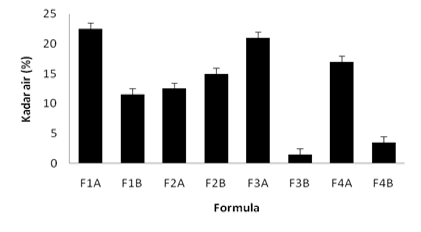
Hasil uji kadar air sabun kertas pencuci tangan pada formula F1A, F1B, F2A, F2B, F3A, F3B, F4A dan F4B berturut-turut adalah 22,5% ± 0,4, 11,5% ± 0,5, 12,5% ± 0,5, 15% ± 0,4, 21% ± 1,17, 1,5% ± 0,1, 17% ± 0,55, 3,5% ± 0,3. Parameter untuk nilai uji kadar ait pada sabun pencuci tangan menurut SNI 1996 adalah tidak melebihi 60% sehingga keseluruhan formula memenuhi persyaratan parameter SNI yang baik
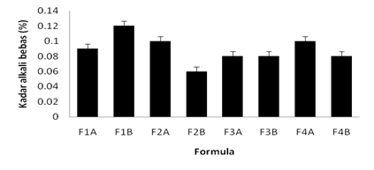
Pengujian Kadar Asam Lemak dan Kadar Alkali Bebas
Pada saat pengujian asam lemak bebas dan alkali bebas menghasilkan sabun kertas positif yang mengandung alkali bebas ketika ditambahkan indikator phenolptaelin pada saat pemanasan terjadi perubahan warna yang membuktikan bahwa alkali bebas terdapat pada sabun. Hal ini terjadi karena alkali bebas tidak bereaksi sempurna dengan asam lemak (proses penyabunan). Hasil uji kadar alkali dan asam lemak bebas sabun pencuci tangan pada formula F1A, F1B, F2A, F2B, F3A, F3B, F4A dan F4B berturut-turut adalah 0,09% ± 0,009, 0,12% ± 0,04, 0,1% ± 0,02, 0,06% ± 0,04, 0,08% ± 0,03, 0,08% ± 0,02, 0,1% ± 0,01, 0,08% ± 0,04. Parameter untuk nilai uji kadar asam lemak dan alkali bebas menurut SNI 06-3532-1994 dimana jumlah alkali bebas tidak melebihi 0,1%, namun pada formula F1B melebihi batas ketetapan SNI yang dapat menyebabkan iritasi pada kulit.
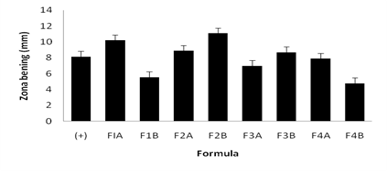
Uji Aktivitas Antibakteri
Pada uji aktifitas antibakteri sabun kertas pencuci tangan dengan pembanding kontrol positif sabun kertas yang beredar dipasaran untuk mengetahui zona hambat terbaik terhadap bakteri Staphylococcus aureus. Zona hambat yang dihasilkan oleh F1A, F2A, F3A, F4A sebagai kontrol negatif mendapat kan hasil berturut-turut adalah 10,2 mm ± 2,94, 8,9 mm ± 4,44, 7 mm ± 1,20, 7,9 mm ± 3,38 sedangkan untuk formulasi sabun kertas yang menggunakan ekstrak metanol daun sungkai pada formula F1B, F2B, F3B dan F4B mendapatkan hasil berturut-turut adalah 5,55 mm ± 5,45, 11,1 mm ± 2,60, 8,69 mm ± 2,43, 4,8 mm ± 0,83.
Analisa Data
Pada penelitian ini akan dilakukan analisa terhadap sabun kertas ektrak metanol daun sungkai yang meliputi organoleptik, kadar air, jumlah alkali dan lemak bebas menurut SNI 06-3532-1994 dan tingkat keasaman sabun (pH) menurut SNI No. 06-4085-1996, serta data daya hambat kertas terhadap pertumbuhan Staphylococcus aureus diolah dan dianalisa dengan menggunakan metode one way Anova pada program SPSS.
Tabel 3. Hasil Analisa Data Normalitas.
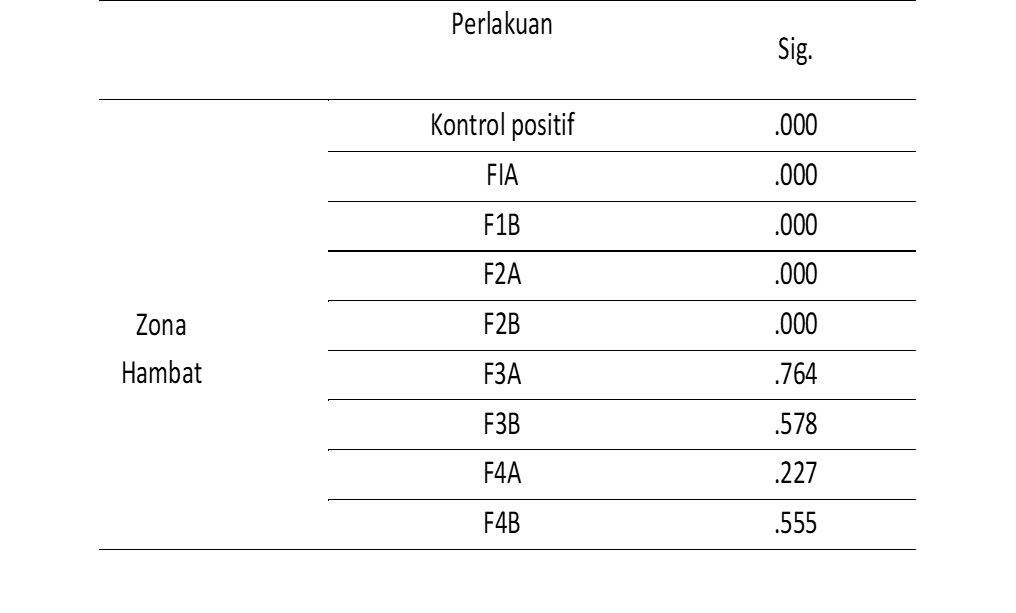
Sig < 0,05 = Data tidak terdisitribusi normal
Tabel 4. Hasil Uji Homogenitas

Sig < 0,05 = Tidak homogeny
Tabel 5. Hasil Uji Kruskal-Wallis

Sig < 0,05 = Terdapat perbedaan
Pembahasan
Pada penelitian ini menggunakan tumbuhan sungkai, dimana tumbuhan sungkai memiliki berbagai manfaat salah satunya sebagai antibakteri [3]. sebelum dilakukan pengujian, tumbuhan sungkai dilakukan determinasi terlebih dahulu tujuannya untuk memastikan tumbuhan yang digunakan adalah benar merupakan spesies Peronema canescens Jack. Sampel ini diekstraksi dengan metode maserasi menggunakan pelarut metanol 95%, dikarenakan metode ini sangat sederhana, cepat dan biaya yang cukup murah. Pemilihan metanol 95% sebagai pelarut karena bersifat semi polar dimana pelarut ini memiliki kemampuan menyaring kelompok senyawa polar dan non polar serta metanol 95% dapat menarik senyawa flavonoid secara optimum [16].
Hasil penelitian daun sungkai (Peronema canescens Jack) yang telah dikeringkan lalu dilakukan maserasi dan kemudian dilakukan ekstraksi dan mendapatkan hasil ekstrak kental dengan rendemen sebesar 13,71% yang menunjukkan nilai rendemen tersebut telah sesuai dengan standar Farmakope Herbal Indonesia edisi II yaitu untuk tanaman famili Lamiaceae memiliki rendemen tidak kurang dari 10% [17].
Skrining fitokimia dilakukan pada ekstrak kental, dengan menunjukkan hasil adanya senyawa alkaloid, flavonoid, saponin, tanin dan steroid. Senyawa alkaloid memiliki kemampuan sebagai antibakteri dan mekanisme penghambatan dengan cara menganggu komponen penyusun peptidoglikan pada sel bakteri sehingga lapisan dinding sel tidak terbentuk secara utuh dan menyebabkan kematian sel tersebut. Selain itu alkaloid juga menghambat pembentukan sintesis protein sehingga dapat menganggu metabolisme bakteri. Golongan senyawa alkaloid dapat menghambat pertumbuhan bakteri gram positif maupun gram negatif sehingga dapat membunuh kuman yang ada ditangan [18].
Hasil pemeriksaan bahan dapat dilihat pada Lampiran 6, berdasarkan Farmakope Indonesia dan Handbook of Pharmaceutical Exipient telah sesuai dengan literatur [19]. Formula sabun kertas pencuci tangan terdiri dari ekstrak daun sungkai (Peronema canescens Jack), HPMC, PVA, Gliserin, Sodium lauryl sulfate, NaOH 50% dalam air, Dinatrium EDTA, dan aquadestilata. Ekstrak daun sungkai sebagai zat aktif berfungsi sebagai antibakteri, HPMC dan PVA digunakan sebagai polimer pembanding, gliserin digunakan sebagai humektan yang berfungsi untuk menjaga kelembaban dan dapat mempertahankan air pada sediaan, NaOH 50% digunakan sebagai saponin agent yang berfungsi sebagai zat pembersih yang digunakan pada sediaan sabun, sodium lauryl sulfate digunakan sebagai surfaktan yang berfungsi untuk menurunkan tegangan permukaan air, dinatrium EDTA digunakan sebagai bahan pengawet dan aqudestilata digunakan sebagai pelarut [19].
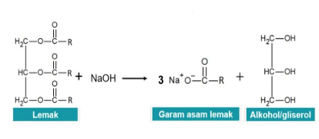
Ekstrak metanol daun sungkai kemudian diformulasikan menjadi sabun kertas pencuci tangan. Sabun mengalami proses saponifikasi karena terjadi reaksi lemak atau gliserida terhadap basa. Sabun ialah hasil hidrolisis asam lemak dan basa. Lemak dan sabun dari asam lemak jenuh rantai panjang (C16-C18) akan terbentuk sabun kertas, dan minyak dari asam lemak tak jenuh rantai pendek (C12-C14) akan terbentuk sabun yang lunak dan mudah larut [20].
Sabun kertas pencuci tangan selanjutnya dilakukan uji evaluasi. Hasil uji organoleptis yang didapatkan pada F1A, F2A, F3A, dan F4A (basis) berwarna putih tulang, berbau khas sedikit tajam, untuk sediaan F1A dan F2A memiliki tekstur yang tipis dan elastis sedangkan pada sediaan F3A dan F4A memiliki tekstur sediaan yang tipis dan kaku, dan untuk sediaan formulasi sabun yang mengandung ekstrak metanol daun sungkai pada F1B, F2B, F3B dan F4B memiliki bau khas sungkai, untuk sediaan F1B dan F3B memiliki warna hijau yang lebih muda dibandingkan dengan F2B dan F4B, hal ini disebabkan pengaruh konsentrasi pada polimer yang terdapat di dalam masing-masing formula dikarenakan polimer HPMC dan PVA berfungsi sebagai pengikat ekstrak daun sungkai, oleh karena itu semakin tinggi konsentrasi polimer maka semakin pekat warna yang dihasilkan pada sediaan. Sedangkan untuk tekstur sediaan dari masing-masing formula sabun kertas ekstrak metanol daun sungkai tidak sama, untuk F1B dan F2B memiliki tekstur yang tipis dan elastis serta untuk F3B dan F4B memiliki tekstur yang tipis dan kaku. Hal ini dikarenakan basis yang digunakan pada pembuatan sabun kertas yaitu polimer HPMC dan PVA, yang mana Polivinil Alkohol (PVA) merupakan sintesis dari polivinil asetat. PVA dapat membentuk lapisan film yang kuat tetapi sifatnya cenderung kaku. Kerugian dari penggunaan polimer PVA inilah yang menjadi faktor mengapa sediaan yang dihasilkan menjadi kaku dan sedikit keras sedangkan polimer HPMC memiliki sifat yang cenderung dapat membentuk film dengan baik maka dari itu polimer HPMC lebih elastis dibandingkan dengan polimer PVA [21]. Maka dapat disimpulkan bahwasannya formula sediaan yang lebih bagus yaitu pada formula F1B dan F2B.
Pengujian pH bertujuan untuk melihat tingkat keasaman sediaan sehingga menjamin sediaan tidak menyebabkan iritasi pada kulit [22]. Hasil rata-rata uji pH pada sediaan sabun kertas pencuci tangan pada F1A didapatkan nilai pH yaitu 7,3, pada F1B didapatkan nilai pH yaitu 7,8, pada F2A didapatkan nilai pH yaitu 7,2, pada F2B didapatkan nilai pH yaitu 7,1, pada F3A didapatkan nilai pH yaitu 7,6, pada F3B didapatkan nilai pH yaitu 7,3, pada F4A didapatkan nilai pH yaitu 7,7, dan pada F4B didapatkan nilai pH sebesar 7,1. Parameter untuk nilai pH pada sabun pencuci tangan menurut SNI 06-4085-1996 adalah 6 – 8 (SNI, 2017), sehingga dari keseluruhan formula sudah memenuhi parameter pH yang baik sebagai sediaan sabun pencuci tangan.
Hasil uji tinggi dan kestabilan busa pada sediaan sabun kertas pencuci tangan memiliki hasil pada F1A sebesar 89,4%, pada F1B memiliki hasil sebesar 94,9%, pada F2A memiliki hasil sebesar 93,9%, pada F2B memiliki hasil sebesar 94,2%, pada F3A memiliki hasil sebesar 93,0%, pada F3B memiliki hasil sebesar 93,8%, pada F4A memiliki hasil sebesar 94,6% dan pada F4B memiliki hasil sebesar 93,8%. Dari hasil tersebut menunjukkan bahwasannya nilai stabilitas busa yang berbeda-beda setiap perlakuan. Perbedaan kestabilan busa antar formula dipengaruhi oleh goncangan pada saat melakukan uji dan konsentrasi sediaan pada masing-masing formula juga mempengaruhi perbedaan kestabilan busa. Pada tinggi busa yang mengandung kosentrasi polimer HPMC lebih tinggi dibandingkan dengan polimer PVA, hal ini disebabkan karena struktur HPMC mengentalkan serta menguatkan dinding gelembung busa dan memperlambat aliran air, menghasilkan busa yang terbentuk lebih padat dan stabil [23]. Pada formula yang mengandung ekstrak daun sungkai memiliki tinggi busa yang lebih besar dibandingkan dengan formula basis, hal ini disebabkan oleh kandungan senyawa saponin yang terdapat pada ekstrak daun sungkai sehingga busa yang dihasilkan lebih tinggi. Disamping itu juga kestabilan busa yang terbentuk akan lama bertahan kemudian busa yang dihasilkan akan berkurang. Campuran yang mengandung bahan aktif sabun akan menghasilkan busa yang stabil bila dicampur dengan air [24].
Hasil uji kadar air sabun kertas pencuci tangan pada formula F1A, F1B, F2A, F2B, F3A, F3B, F4A dan F4B berturut-turut adalah 22,5%, 11,5%, 12,5%, 15%, 21%, 1,5%, 17%, 3,5%. Berdasarkan hasil yang diperoleh kadar air yang dihasilkan, semakin besar konsentrasi pada bahan maka semakin kecil persentase kadar air yang didapatkan. Kadar air yang tinggi juga dapat dipengaruhi oleh bahan-bahan yang bersifat higroskopis yaitu seperti SLS, gliserin dan juga dapat dipengaruhi oleh penambahan aquadest [12].
Evaluasi sabun kertas pencuci tangan selanjutnya melakukan uji kadar asam lemak dan alkali bebas. Tujuan dari evaluasi ini untuk mengetahui dan melihat kadar asam lemak serta alkali bebas yang terdapat pada sediaan sabun. Apabila sediaan sabun yang menghasilkan asam lemak bebas akan mengurangi daya pembersihan, sedangkan jika sediaan sabun menghasilkan alkali bebas maka akan menyebabkan iritasi pada kulit dan akan menyebabkan kulit menjadi kering [25]. Pada saat pengujian asam lemak bebas dan alkali bebas menghasilkan sabun kertas positif yang mengandung alkali bebas ketika ditambahkan indikator phenolptaelin pada saat pemanasan terjadi perubahan warna yang membuktikan bahwa alkali bebas terdapat pada sabun. Hal ini terjadi karena alkali bebas tidak bereaksi sempurna dengan asam lemak (proses penyabunan). Hal ini disebabkan oleh pada saat proses evaluasi menggunakan metode titrimetri yang dapat mempengaruhi kadar alkali bebas dimana terdapat beberapa kelemahan yaitu, alat pengukur volume seperi buret, pipet ukur dan alat lainnya tidak terkalibrasi serta tingkat kemurnian baku primer tidak tervalidasi sehingga hal tersebut dapat mempengaruhi hasil [26]. Pada hasil evaluasi tersebut terlihat formula sabun memenui persyaratan kadar alkali bebas menurut SNI 06-3532-1994 dimana jumlah alkali bebas tidak melebihi 0,1%, namun pada hasil F1B memiliki nilai alkali bebas melebihi syarat SNI 06-3532-1994 yaitu diatas 0,1%. Hal ini dikarenakan jumlah alkali yang tidak tervalidasi baik pada pipet ukur saat proses pembuatan sabun sehingga nilai yang dihasilkan tidak memenuhi persyaratan. Kelebihan alkali bebas dapat menyebabkan iritasi pada kulit [27].
Pada uji aktifitas antibakteri sabun kertas pencuci tangan dengan pembanding kontrol positif sabun kertas yang beredar dipasaran untuk mengetahui zona hambat terbaik terhadap bakteri Staphylococcus aureus . Zona hambat yang dihasilkan oleh F1A, F2A, F3A, F4A sebagai kontrol negatif mendapat kan hasil dengan rata-rata berkisar antara 7 mm – 10,2 mm, sedangkan untuk formulasi sabun kertas yang menggunakan ekstrak metanol daun sungkai seperti pada formula F1B, F2B, F3B dan F4B mendapatkan hasil dengan rata-rata berkisar antara 4,8 mm – 11,1 mm. Hasil zona hambat pada pengujian formulasi sabun kertas ekstrak metanol daun sungkai lebih besar dibandingkan dengan formula basis sabun kertas pencuci tangan, hal ini disebabkan oleh adanya efektivitas antibakteri karena aktifitas metabolit sekunder yang terkandung dalam ekstrak metanol daun sungkai yaitu senyawa Flavonoid. Flavonoid bekerja sebagai antibakteri dengan membentuk senyawa kompeks terhadap protein ekstraseluler yang mengandung intergritas membran sel bakteri [28]. Hasil ini sesuai dengan penelitian sebelumnya yang dilakukan oleh [3] bahwasannya ekstrak metanol daun sungkai memiliki aktivitas antibakteri. Dari hasil pengujian aktivitas antibakteri dapat dilihat bahwa formula F2B memiliki aktivitas antibakteri lebih bagus dibandingkan dengan formula lainnya dan menunjukan zona hambat yang lebih besar dibandingkan dengan formula lainnya.
Tabel 6. Hasil uji aktivitas antibakteri sediaan sabun kertas pencuci tangan
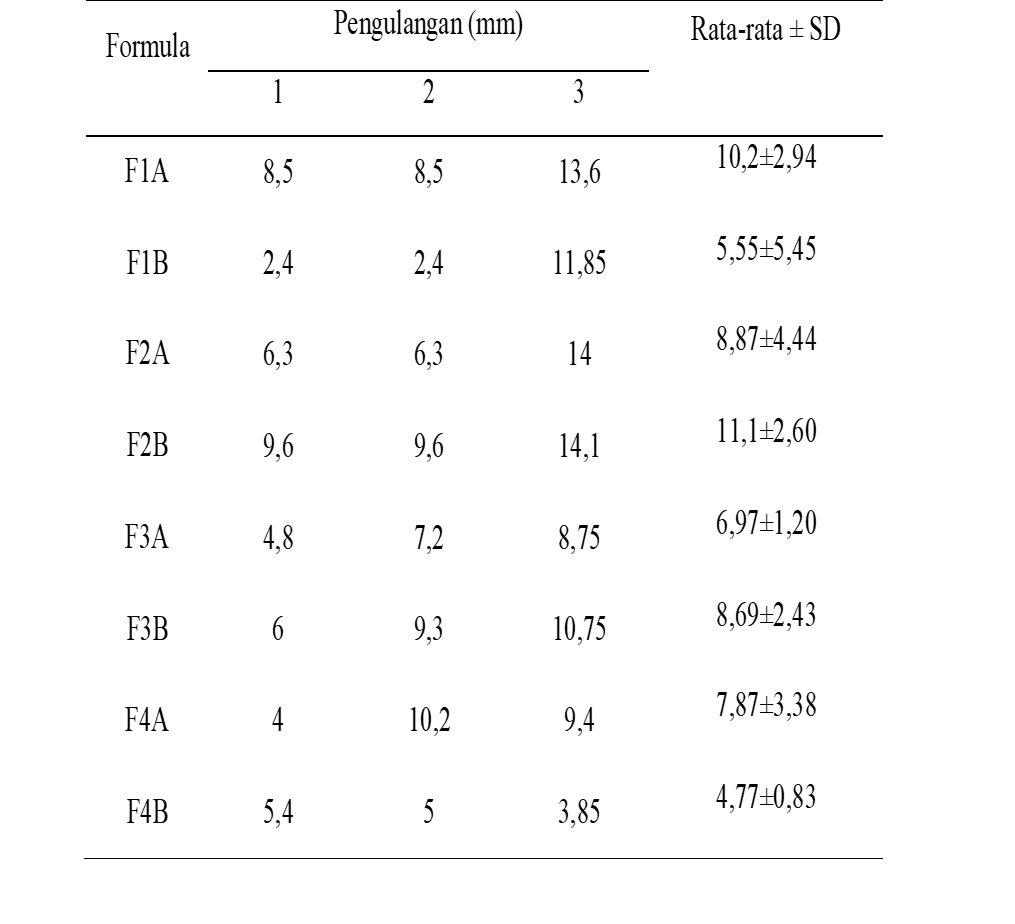
F1A: formula basis sabun dengan konsentrasi HPMC 0,5%
F1B: formula sediaan sabun ekstrak daun sungkai1% dengan konsentrasi HPMC 0,5%
F2A: formula basis sabun dengan konsentrasi HPMC0,75%
F2B: formula sediaan sabun ekstrak daun sungkai1% dengan konsentrasi HPMC 0,75%
F3A: formula basis sabun dengan konsentrasi PVA 1,75%
F3B: formula sediaan sabun ekstrak daun sungkai1% dengan konsentrasi PVA 1,75%
F4A: formula basis sabun dengan konsentrasi PVA 2%
F4B: formula sediaan sabun ekstrak daun sungkai1% dengan konsentrasi PVA 2%.
Pada uji One Way ANOVA menunjukkan hasil dari beberapa perlakukan uji normalitas dan uji homogenitas kurang dari 0,05 yang menandakan bahwasannya data tersebut tidak terdistribusi normal, maka dari itu analisa data kemudian dilakukan uji Kruskal-Wallis yang mana pada nilai yang dihasilkan uji tersebut menunjukkan hasil lebih dari 0,05 yang menandakan bahwasanya data tersebut memenuhi persyaratan Kruskal-Wallis dan tidak menunjukan adanya perbedaan pada masing-masing perlakukan uji.
Kesimpulan
Dari penelitian yang dilakukan dapat disimpulkan sebagai berikut :
Formulasi sediaan sabun kertas yang menghasilkan formula terbaik yaitu dengan menggunakan konsentrasi HPMC 0,75% sedangkan sabun kertas yang menggunakan PVA menghasilkan sediaan yang kurang baik. Konsentrasi minimal ekstrak metanol daun sungkai yang dapat menghambat bakteri Staphylococcus aureus dan dapat dijadikan sediaan sabun kertas pencuci tangan yaitu dengan konsentrasi 1%.
Daftar Pustaka
[1] D. Nurahmanto, I. R. Mahrifah, R. F. N. Azis, and V. A. Rosyidi, “Formulasi Sediaan Gel Dispersi Padat Ibuprofen : Studi Gelling Agent dan Senyawa Peningkat,” J. Ilm. Manuntung, vol. 3, no. 1, pp. 96–105, 2017
[2] A. Arifin, Sartini, and Marianti, “Evaluasi Karakteristik Fisik Dan Uji Permeasi Pada Formula Patch Aspirin Menggunakan Kombinasi Etilselulosa Dengan Polivinil pirolidon,” J. Sains Dan Kesehat., vol. 2, no. 1, pp. 40–49, 2019
[3] A. Ibrahim and H. Kuncoro, “Identifikasi Metabolit Sekunder dan Aktivitas Antibakteri Ekstrak Daun Sungkai (Peronema canescens Jack) terhadap Beberapa Bakteri Patogent,” J. Trop. Pharm. Chem., vol. 2, no. 1, pp. 8–18, 2012.
[4] A. Ningsih, Subhan, and N. Djide, PotensiAntimikroba Dan AnalisisSpektroskopiIsolatAktifEkstrak N-HeksanDaunSungkai (Peronemacanescens Jack) TerhadapBeberapaMikrobaUji. Makassar, 2013.
[5] N. P. Pindan, Daniel, C. Saleh, and A. R. Magdaleni, “Uji Fitokimia dan Uji Aktivitas Antioksidan Ekstrak Fraksi n-Heksana Etil Asetat dan Etanol Sisa Daun Sungkai (Peronema canescens Jack) Dengan Metode DPPH,” J. At. FMIPA, vol. 6, no. 1, pp. 22–27, 2020.
[6] R. Alfian and H. Susanti, “Penetapan Kadar Fenolik Total Ekstrak Metanol Kelopak Bunga Rosella Merah (Hibiscus sabdariffa Linn) dengan Variasi Tempat Tumbuh Secara Spektrometri,” J. Ilm. Kefarmasian, vol. 2, no. 1, pp. 73–80, 2012
[7] S. Adlis, “Aktivitas Antibakteri dan Sitotoksik Ekstrak Daun Sungkai (Peronema canescens Jack),” J. Kim. UNAND, vol. 9, no. 4, pp. 303–401, 2020.
[8] M. Suhambangun, O. Datu, G. Tiwow A.R, and N. Patolangi O, “Formulasi Sediaan Sabun Antiseptik Ekstrak Daun Pepaya (Carica papaya),” J. Biofarmasetikal Trop., vol. 2, no. 1, pp. 43–51, 2019.
[9] A. Habibah, G. Cahya, E. Darma, and A. Gadri, “Pengaruh Natrium Alginat dan Hpmc Sebagai Basis terhadap Karakteristik Fisik Sediaan Film Soap yang Mengandung Serai Wangi ( Cymbopogon Winterianus Jowitt .),” Pros. Farm., vol. 3, no. 1, pp. 59–62, 2017.
[10] J. . Harborne, Metode Fitokimia : Penuntun Cara Modern Menganalisis Tumbuhan. Bandung: ITB Press, 1996
[11] A. N. Primadiamanti and M. D. Muslim, “Uji Stabilitas Asetosal Bentuk Sedian Tablet dan Tablet Salut Entrik. Jurnal Analasisi Farmasi,” J. Analasisi Farm., vol. 2, no. 3, pp. 206–213, 2017.
[12] E. Fiskia and C. Mala, “Formulasi Dan Evaluasi Sediaan Sabun Kertas Ekstrak Etanol Fuli Buah Pala(Myritica fragrans Houtt),” vol. 3, no. 2, pp. 120–127, 2021.
[13] I. A. Yulia, FormulasiSediaanSabunMandiPadatEkstrakEtanolDaunAfrika (VernoniaAmygdalina Del.). kupang: Karya Tulis Ilmiah, 2018.
[14] A. Maulana, H. Susilo, and E. Rustiani, “Pembuatan Sabun Transparan Aromaterapi Minyak Atsiri Akar Wangi (Chrysopogon zizanioides (L.)Roberty,” J. FMIPA, vol. 1, no. 1, pp. 1–10, 2013
[15] D. Fransisca, D. . Kahanjak, and A. Frethernety, “Uji aktivitas antibakteri ekstrak etanol daun sungkai (Peronema canescens Jack) terhadap pertumbuhan Escherichia coli dengan metode difusi cakram Kirby-Bauer. J Pengelolaan Lingkung Berkelanjutan,” J. Env. Sustain Manag, vol. 4, no. 1, pp. 460–470, 2020.
[16] S. N. Citra, G. D. Permana, and A. Jambe, “Pengaruh Jenis Pelarut Terhadap Kandungan Total Flavonoid Dan Aktivitas Antioksidan Ekstrak Daun Matoa (Pometia Pinnata),” pp. 1–10, 2020.[17] Departemen Kesehatan RI, Farmakope Herbal Indonesia edisi II. Jakarta, 2017
[18] W. Anggraini, siti choirun Nisa, R. R. DA, and B. M. ZA, “Aktivitas Antibakteri Ekstrak Etanol 96% Buah Blewah (Cucumis melo L. Var. cantalupensis) Terhadap Pertumbuhan Bakteri Escherchia coli,” Pharm. J. Indones., vol. 5, no. 1, pp. 61–66, 2019.
[19] C. R. J. . Rowe and M. E. Quinn, Handbook Of Pharmaceutical Excipients edisi 6. London: Pharmaceutical Press, 2009.
[20] J. . Ralph and S. . Joan, Kimia Organik. Jakarta: Erlangga, 1997.
[21] N. R. Amalia, D. Rahmawanty, and P. H. Ratnapuri, “Pengaruh Variasi Konsentrasi PVA dan HPMC Terhadap Stabilitas Fisik Masker Peel-Off Ekstrak Biji Pepaya (Carica papaya L),” J. Pharmasience, vol. 5, no. 1, pp. 78–85, 2018.
[22] S. B. Astuti, T. Lestari, and V. Nurviana, “Formulasi gel facial wash ekstrak daun hantap (Sterculia coccinea Var. Jack) dan uji aktivitasnya sebagai antioksidan,” Pros. Semin. Nas. Disem. Penelit., vol. 1, pp. 244–255, 2021
[23] H. Hutauruk, P. V. Y. Yamlean, and W. Wiyono, “Formulasi Dan Uji Aktivitas Sabun Cair Ekstrak Etanol Herba Seledri (Apium Graveolens L) Terhadap Bakteri Staphylococcus aureus,” Pharmacon, vol. 9, no. 1, p. 73, 2020.
[24] Y. Anggraeini, F. Nisa, and S. O. Beta, “Karakteristik Fisik dan Aktivitas Antibakteri Sabun Cair Minyak Nilam (Pogostemon cablin Benth) yang Berbasis Surfaktan Sodium Lauril Eter Sulfat,” J. Kefarmasian Indones., vol. 10, no. 1, pp. 1–10, 2020[25] H. C. Handayani, Pengaruh Peningkatan Konsentrasi Ekstrak Etanol 96% Biji Alpukat (Persea americana Mill) Terhadap Formulasi Sabun Padat Transparan. Jakarta: Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah, 2009
[26] Sudjadi, Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar, 2003[27] N. Sadiyah, I. N. Hartati, A. R. Raesta, and L. Kurniasari, “Formulasi Sabun Mandi Padat Berbasis Minyak Biji Kapuk Randu (Ceiba petandra Gaertn) dengan Penambahan Jasmine Oil,” Inov. Tek. Kim., vol. 3, no. 2, pp. 8–11, 2018.
[28] M. W. Mulyani and R. P. Sarjono, “Konsentrasi Hambat Minimum (KHM) Kadar Sampel Alang-alang (Imperata cylindrica) dalam Etanol Melalui Difusi Cakram,” Chem Info, vol. 1, no. 1, pp. 35–42, 2017.
cara mengutip artikel ini
https://jurnal.unpad.ac.id/farmasetika/rt/captureCite/43376/0
 Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3
Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3




