Majalah Farmasetika, 8 (4) 2023, 335-350
https://doi.org/10.24198/mfarmasetika.v8i4.46118
Artikel Pnelitian
Melia Sari*1, Leny2, Astri Cahyani1
1*Departemen Mikrobiologi, Fakultas Farmasi dan Kesehatan, Institut Kesehatan Helvetia, Medan
2Departemen Farmasetika, Farmasi Fakultas Farmasi dan Kesehatan, Institut Kesehatan Helvetia, Medan
*E-mail: msmeliasari@gmail.com
(Submit 29/03/2023, Revisi 31/03/2023, Diterima 26/04/2023, Terbit 23/05/2023)
Abstrak
Kesehatan gigi dan mulut merupakan salah satu peran penting dalam menentukan status kesehatan seseorang. Penyakit gigi dan mulut khususnya karies gigi sering tidak mendapat perhatian dari masyarakat maupun pemerintah karena jarang membahayakan jiwa. Faktor penyebab karies gigi yaitu mikroorganisme, bentuk gigi, makanan, dan waktu. Metode penelitian ini yaitu eksperimental dengan cara metode difusi menggunakan cakram untuk mengatahui zona hambat sediaan obat kumur dari ekstrak etanol daun sisik naga terhadap bakteri Streptococcus mutans dan Streptococcus viridans. Hasil penelitian dari sediaan obat kumur ekstrak daun sisik dari ketiga formula pada uji organoleptis berbentuk cair berwarna coklat bening yang homogen dengan bau minyak kayu manis sedikit mentol dan rasa khas sisik naga diikuti segar dari mentol. Hasil uji pH dari konsentrasi 5%, 10%, 15% yaitu 5,57; 5,66; 5,62. Uji viskositas 5,06; 5,13; 5,19. Uji stabilitas fisik terjadinya perubahan warna, penurunan pH dan viskositas. Uji aktivitas antibakteri sediaan obat kumur ekstrak daun sisik naga pada Streptococcus mutans yaitu 12,16±0,60 mm, 13,78±0,58 mm, 15,26±0,55 mm dan pada Streptococcus viridans 10,78±0,51 mm, 11,8±0,70 mm, 12,86±0,55 mm. Kesimpulan dari penelitian ini yaitu ekstrak daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) dapat diformulasikan dalam bentuk sediaan obat kumur dan memiliki daya hambat terhadap bakteri Streptococcus mutans dan Streptococcus viridans dengan konsentrasi optimum pada konsentrasi 10% dan 15% dengan kategori kuat.
Kata kunci: Karies gigi, Sisik Naga, Streptococcus mutans, Streptococcus viridans
Teks Lengkap:
Pendahuluan
Kesehatan gigi dan mulut merupakan salah satu peran penting dalam menentukan status kesehatan seseorang. Untuk menilai status kesehatan gigi, dapat dilihat dari ada tidaknya penyakit gigi, salah satunya adalah karies gigi (1). Penyakit gigi dan mulut khususnya karies gigi sering tidak mendapat perhatian dari masyarakat ataupun pemerintah karena jarang membahayakan jiwa. Padahal, kesehatan gigi mempunyai peran penting dalam upaya meningkatkan derajat kesehatan masyarakat (2). Karies gigi merupakan gangguan kesehatan gigi dan mulut. Karies gigi terjadi akibat adanya kerusakan jaringan keras gigi pada enamail, dentil, dan sementum (3). Ada beberapa cara pengendalian dari permasalahan gigi dan mulut, salah satunya yaitu menggunaan obat kumur. Obat kumur berperan penting dalam kebersihan mulut seorang, obat kumur membantu untuk meringankan gejala gingivitis, sariawan, bau mulut, dan juga bisa diandalkan untuk merusak bakteri patogen pada mulut (4).
Pada rongga mulut seseorang terdapat berbagai macam bakteri, salah satunya yaitu Streptococcus mutans bakteri kariogenik yang merupakan penyebab utama karies gigi (5). Streptococcus viridans juga merupakan salah satu bakteri yang dapat menyebabkan karies gigi. Bakteri ini merupakan flora normal yang menghuni rongga mulut dan saluran nafas manusia bagian atas (6). Streptococcus mutans dan Streptococcus viridans merupakan bakteri yang bersifat kariogenik tersebut akan mempermentasi sukrosa menjadi asam laktat (7).
Faktor-faktor yang dapat mempengaruhi Pertumbuhan dan perkembangan bakteri yaitu nutrisi, pH, temperature, oksigen dan tekanan osmosis (8). Uji aktivitas antibakteri dapat menggunakan beberapa metode, salah satunya metode difusi. Prinsip kerja metode difusi adalah terdifusinya senyawa antibakteri ke dalam media padat dimana mikroba uji telah diinokulasikan. Hasil pengamatan yang diperoleh berupa ada atau tidaknya daerah zona bening yang terbentuk di sekeliling kertas cakram yang menunjukan zona hambat pertumbuhan bakteri (9).
Proses pencarian obat sebagai antibakteri yang berasal dari sumber daya alam terus-menerus dikembangkan. Adapun dikarenakan pengunaan antibiotik untuk pengobatan infeksi mengalami permasalahan dalam hal resistensi (10). Resistensi terhadap antibiotik mempengaruhi aktivitas dan perkembangan bakteri, penanggulangan secara alami dapat dengan memanfaatkan ekstrak tanaman sebagai salah satu alternatif yang dapat dimanfaatkan untuk menghambat pertumbuhan dan membunuh agen penyebab penyakit (11).
Salah satu tanaman yang banyak tumbuh didataran Indonesia adalah sisik naga (Pyyrosia piloselloides). Tanaman ini memiliki sinonim Drymoglossum piloselloides (L.) C. Presl (10). Epifit merupakan tumbuhan yang hidup menempel pada batang atau dahan tanpa mengambil makanan dari inangnya. Manfaat tumbuhan epifit selain untuk keperluan media pembelajaran yang dapat diteliti dan dipelajari, nilai manfaat tumbuhan paku epifit juga dapat digunakan sebagai tanaman hias, kerajinan maupun obat-obatan (12). Sisik naga (Drymoglossum pilloseloides (L.) C. Presl) adalah salah satu tanaman
yang dapat digunakan sebagai tanaman obat. Bagian sisik naga yang banyak diteliti sebagai bahan obat yaitu daunnya yang dijadikan simplisia (6). Salah satu cara menjamin mutu simplisia adalah dengan melakukan standarisasi simplisia. Parameter mutu simplisia meliputi kadar air, kadar sari dalam air, kadar sari larut dalam etanol, kadar abu total, kadar abu tidak larut asam (13).
Pada penelitian sebelumnya oleh Ulfa, sampel telah diuji pada judul “Aktivitas Antibakteri Dan KLT Bioautografi Ekstrak Etanol Daun Sisik Naga (Drymoglossum piloselloides) Terhadap Streptococcus mutans” dimana pada uji KLT konsentrasi 12,5 diketahui adanya hambatan terhadap S. mutans yang ditandai oleh daerah bening dengan diameter rata-rata 16,5 mm terlihat pada titik penotolan ekstrak (14). Pada penelitian “Uji Aktivitas Antioksidan Dan Antibakteri Dari Ekstrak Kasar Metanol Daun Sisik Naga (Drymoglossum piloselloides (L) Presl )”. Tumbuhan ini memiliki kandungan flavonoid, fenol, dan terpenoid/steroid pada uji skrining fitokimia (15). Pada penelitian Rizka Rahmaningtyas hasil skrining fitokimia ektrak daun sisik naga dengan pelarut etanol dan fraksi etil asetat positif flavonoid, tannin, dan triterpenoid/steroid, dan uji antibakteri dengan konsentrasi 10% dengan rata-rata zona hambat 19 mm pada Staphylococcus aureus (16).
Metode
Penelitian ini dilakukan menggunakan metode eksperimental dengan tahapan penelitian: pengumpulan sampel, pembuatan simplisia, pembuatan ekstrak, skrining fitokimia, pembuatan sediaan obat kumur dan uji aktivitas antibakteri sediaan obat kumur terhadap Streptococcus mutans dan Streptococcus viridans.
Alat
Alat yang digunakan meliputi Aluminium foil (Klinpak), kertas saring, blender (Philips), timbangan digital, rotary evaporator (Heidolph), alat-alat gelas (Pyrex), kain kasa (Onemed), cawan porselin, kurs porselin, pH meter (Xingweiqiang), penangas air (B-ONE), cawan petri (Pyrex), jangka sorong (Nankai), autoklaf (Tomy), lemari pendingin (LG), oven (Memmert), inkubator (Memmert), laminary airflow (Esco), wadah sediaan obat kumur.
Bahan
Bahan yang digunakan meliputi Daun sisik naga, etanol 70%, zink klorida (Merck), mentol, PEG-40 hydrogenated castrol oil, gliserin (Onemed), minyak kayu manis, aquadest, larutan NaCl 0,9%, TYCSB (Himedia), MHA (Himedia), HCl 2N, H2SO4, kloroform, FeCl3 1%, reaksi mayer, reagen bouchardat, reagen dragondrof,
obat kumur enkasari, serta bakteri Streptococcus mutans dan Streptococcus viridans yang diperoleh dari Laboratorium Mikrobiologi Fakultas Farmasi Universitas Sumatera Utara.
Prosedur Rinci
1. Pembuatan Simplisia Dan Ekstrak Daun Sisik Naga
Sebanyak 12 kg daun sisik naga ditimbang, kemudian dicuci, dirajang, ditiriskan, dan dikeringkan dilemari pengering suhu <60ºC, setelah kering ditimbang, dihaluskan, dan diayak mesh 40 diperoleh serbuk simplisia (17). Kemudian diambil sebanyak 900 gram serbuk simplisia daun sisik naga dimaserasi dengan pelarut etanol 70% sebanyaK 9 L. Pertama serbuk simplisia dimasukan kedalam wadah, lalu direndam dalam 75 bagian etanol 70% sebanyak 6.750 mL, kemudian ditutup dengan almunium foil selama 5 hari, sesekali diaduk. Setelah itu disaring untuk mendapatkan maserasi pertama, ampas kemudian direndam kembali dalam 25 bagian etanol 70% sebanyak 2.250 mL, kemudian didiamkan selama 2 hari, sesekali diaduk. Setelah itu disaring untuk mendapatkan maserasi kedua. Hasil maserasi pertama dan maserasi kedua kemudian digabungkan dan dipekatkan dengan menggunakan rotary evaporator suhu 45ºC dan diperoleh ekstrak kental (18).
2. Karakteristik Simplisia
Karakteristik simplisia meliputi :
a. Penetapan Kadar Air
Penetapan kadar air simplisia dilakukan dengan cara gravimetri. Botol timbang dikeringkan pada oven 105°C selama 30 menit dinginkan pada eksikator selama 15 menit. Ditimbang serbuk simplisia sisik naga dengan masing-masing 3 gram dimasukan kedalam botol timbang, dipanaskan 105°C selama 1 jam didinginkan dalam esikator 15 menit menit hingga berat konstan.
b. Penetapan Kadar Sari Dalam Air
Ditimbang 5 gram serbuk simplisia, dimaserasi selama 24 jam dalam 100 mL air- kloroform (2,5 mL kloroform dalam air suling 1000 mL) dalam labu tersumbat sambil sekali-kali dikocok. Disaring dan diambil 20 mL filtrat diuapkan hingga kering dalam cawan penguap, dipanaskan pada suhu 105°C hingga bobot tetap.
c.Penetapan Kadar Sari Larut Dalam Etanol
Ditimbang 5 gram serbuk simplisia, dimaserasi dalam 100 mL etanol 95% selama 24 jam dalam labu tersumbat, sambal sekali-kali dikocok dan disaring. Sebanyak 20 mL filtrat diuapkan diatas penangas air sampai kering, kemudian dipanaskan pada suhu 105°C hingga bobot konstan.
d. Penetapan Kadar Abu Total
Ditimbang serbuk simplisia 3 gram dimasukan ke dalam krus porselin yang telah dipijar dan ditara, kemudian dipanaskan menggunakan tanur selama 3 jam suhu 600°C. Sampel hasil pemijaran didinginkan pada eksikator 15 menit dan ditimbang untuk mendapatkan bobot konstan.
E. Penetapan Kadar Abu Tidak Larut Asam
Abu hasil pemijaran dari abu total dididihkan dengan mengunakan 25 mL asam klorida 2 N encer selama 5 menit. Abu yang tidak larut dengan asam dikumpulkan, disaring dan ditimbang. Residu dipijarkan, kemudian didinginkan dan ditimbang untuk mendapatkan bobot konstan (19).
3. Skrining Fitokimia
Skrining fitokimia meliputi :
A. Uji Alkaloid
Ekstrak 0,5 gram dilarutkan dengan 1 mL HCL 2N, ditambahkan 9 mL aquadest dan panaskan 2 menit, dinginkan kemudian saring. Filtrat dibagi ke dalam 3 tabung reaksi, tabung 1 ditambahkan 1-3 tetes pereaksi Mayer menghasilkan endapan putih atau kuning menandakan adanya alkaloid, tabung 2 ditambahkan 1-3 tetes pereaksi Dragendroff menghasilkan warna endapan merah bata atau jingga menandakan adanya alkaloi, tabung 3 ditambahkan 1-3 tetes pereaksi bouchardat endapan coklat hitam menandakan adanya alkaloid.
B. Uji Flavonoid
Mg + HCl
Sebanyak 1 mL ektrak dilarutkan dengan 5 mL air panas kemudian saring, Filtrat ditambahkan 0,1 mg serbuk Mg dan ditambahkan 1 ml HCl pekat lalu masukan 1 mL amil alcohol, reaksi positif jika terbentuk warna merah, kuning, jingga pada lapisan amil `
Zn + HCl
Sebanyak 1 mL ektrak dilarutkan dengan 5 ml air panas kemudian saring. Filtrat ditambahkan 0,5 serbuk Zn, ditambahkan 2 mL HCl 2N. Didiamkan selama 1 menit dan ditambahkan 5 mL HCl pekat. Positif jika terbentuk warna merah (20).
C. Uji Saponin
Ekstrak sebanyak 0,5 gram dimasukan kedalam tabung reaksi, ditambahkan dengan 10 mL aquadest dan dikocok. Jika terbentuk busa yang stabil (1 cm – 10 cm) dan pada penambahan 1 tetes HCl 2 N buih tidak hilang menunjukan adanya saponin.
D. Uji Tanin
Ekstrak sebanyak 0,5 gram dimasukan ke dalam tabung reaksi, lalu diencerkan dengan aquadest sampai tidak berwarna kemudian diaduk, hasil pengenceran di ambil 2 mL ditambahkan FeCl3 1% sebanyak 3 tetes, menghasilkan biru atau hijau, kehitaman menunjukan adanya tannin.
E. Uji Triterpenoid/Steroid
Ekstrak 1 gram dimaserasi dengan 20 mL N-heksan selama 2 jam dan saring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan 2 tetes asam asetat anhidrat dan 1 tetes H2SO4 pekat. Jika terbentuk warna merah coklat atau ungu menunjukan adanya terpenoid dan terbentuk warna hijau atau biru menunjukan adanya steroid (21).
Formulasi Obat Kumur
Formulasi obat kumur dapat dilihat pada tabel 1.
Tabel 1. Formulasi Modifikasi Sediaan Obat Kumur
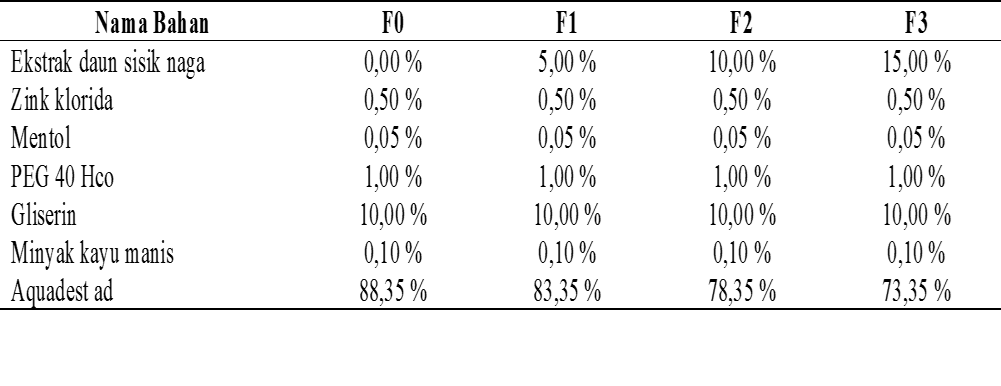
Keterangan :
F0 : Blanko
F1 : Konsentrasi 5%
F2 : Konsentrasi 10%
F3 : Konsentrasi 15%
4. Pembuatan Obat Kumur
Siapkan alat dan bahan yang digunakan untuk pembuatan sediaan obat kumur. Ditimbang semua bahan yang digunakan, larutkan zink klorida dalam sebagian air (larutan 1). Campurkan PEG-40, mentol, gliserin dan minyak kayu manis jadi satu (larutan 2). Tambahkan larutan 1 pada larutan 2 perlahan-lahan sambil diaduk. Setelah itu, tambahkan ekstrak daun sisik naga, aduk. Tambahkan sisa air sampai 450 mL, saring dan masukan dalam botol sediaan (22).
5. Evaluasi Obat Kumur
Evaluasi Obat Kumur meliputi :
a. Uji organoleptis dilakukan dengan menggunakan panca indera dengan cara melihat bentuk, homogenitas, bau, rasa dan warna dari sediaan obat kumur yang telah di buat (23).
b. Uji viskositas Sediaan diambil sebanyak 50 mL masukan dalam beaker glass, atur rotor No. 2 dengan kecepatan 60 rpm. Kemudian sampel dicelupkan sampai tanda batas rotor. Viskometer dinyalakan selama 10 detik, dan setelah itu nilai viskositas akan muncul di layar viscometer (24).
c. Pengukuran pH dilakukan terhadap sediaan obat kumur, kalibrasi terlebih dahulu dalam larutan buffer pH 7 dan pH 4, setelah itu diambil 30 mL sampel dimasukan kedalam beaker, masukan PH meter kedalam sampel sampai didapatkan nilai pH yang konstan (25).
d. Uji stabilitas sediaan dilakukan dengan metode stress condition dengan penyimpanan 5°C dan 35ºC selama 6 siklus selama 1 bulan.
6. Pengujian Aktivitas Antibakteri
Pengujian antibakteri menggunakan metode cakram, diambil bakteri uji sebanyak 0,5 mL dimasukan ke dalam cawan petri dan dimasukan media MHA sebanyak 20 mL. Kemudian larutan uji dengan masing-masing konsentrasi 5%, 10%, 15% diambil sebanyak 50 µL lalu ditetesin pada kertas cakram, diletakkan diatas media. Kemudian diinkubasi pada suhu 37°C selama 1 x 24 jam, diamati zona bening disekitar cakram dan diukur menggunakan jangka sorong (26).
Hasil dan Pembahasan
Hasil Simplisia dan Ekstrak Daun Sisik Naga
Hasil pembuatan simplisia dari daun sisik naga sebanyak 12 kg diperoleh serbuk simplisia 1.330 gram dan diperoleh ekstrak kental sebanyak 148,33 gram dengan randemen sebesar 16,48%.
Hasil Pemeriksaan Karakteristik Simplisia Daun Sisik Naga
Hasil pemeriksaan karakteristik simplisia dapat dilihat pada tabel 2 di bawah ini.
Tabel 2. Hasil Pemeriksaan Karakteristik Serbuk Simplisia Daun Sisik Naga
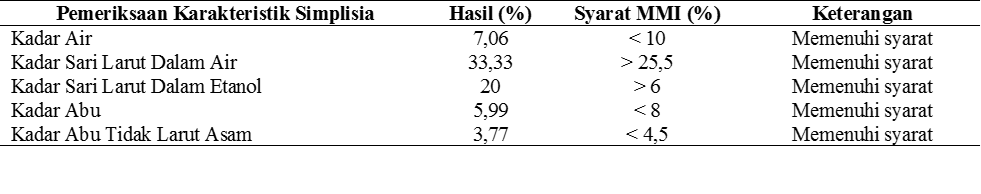
Berdasarkan hasil yang didapat, Materia Medika Indonesia merupakan acuan untuk menentukan standart mutu simplisia daun sisik naga. Penetapan kadar air pada simplisia bertujuan untuk mengetahui kandungan air yang terdapat pada simplisia dengan cara gravimetri. Dimana air merupakan media tempat tumbuhnya mikroba
sehingga akan merusak simplisia , persyaratan mutu kadar air menurut MMI yaitu < 10%. Hasil dari penetapan kadar air pada simplisia daun sisik naga yaitu 7,06% memenuhi syarat.
Penetapan kadar sari larut dalam air pada simplisia bertujuan untuk mengetahui jumlah senyawa yang dapat tersari dalam pelarut air. Dengan cara penyarian mengunakan air dan metode maserasi serta gravimteri. Persyaratan mutu kadar sari larut dalam air menurut MMI yaitu >25,5%. Hasil dari penetapan kadar sari larut dalam air yaitu 33,33% memenuhi syarat. Penetapan kadar sari larut dalam etanol pada simplisia bertujuan untuk mengetahui jumlah senyawa yang dapat tersari dalam pelarut etanol. Dengan cara penyarian menggunakan pelarut etanol 96% dan metode maserasi serta gravimetri. Persyaratan mutu kadar sari larut dalam etanol menurut MMI yaitu >6%. Hasil dari penetapan kadar sari larut dalam etanol yaitu 20% memenuhi syarat.
Penetapan kadar abu total dan kadar abu tidak larut asam pada simplisia bertujuan memberikan gambaran kandungan mineral internal dan eksternal, Sampel dipanaskan pada temperature 600°C dimana senyawa organic terdektruksi dan menguap sehingga tinggal unsur mineral dan anorganik. Persyaratan mutu kadar abu total menurut MMI yaitu <8%. Hasil dari penetapan kadar abu total yaitu 5,99% memenuhi syarat. Persyaratan mutu kadar abu tidak larut asam menurut MMI yaitu <4,5%, Hasil dari penetapan kadar abu tidak larut asam 3,77% memenuhi syarat (27).
Hasil Skrining Fitokimia
Hasil pemeriksaan skrining fitokimia dapat dilihat pada tabel 3.
Tabel 3. Hasil Skrining Fitokimia

Hasil dari penelitian ini pada uji alkaloid didapatkan positif endapan putih dengan preaksi mayer, prekasi dragendrof tidak terbentuk endapan merah bata, dan prekasi bouchardat positif endapan coklat. Apabila terdapat endapan paling sedikit 2 atau 3 dari pengujian, menandakan bahwa ekstrak daun sisik naga mengandung senyawa alkaloid.
Hasil dari uji flavonoid pada penelitian ini didapatkan pada penambahan mg warna kuning pada lapisan amil alcohol, dan pada penambahan zn terdapat warna merah intensif, menandakan adanya senyawa flavonoid pada ekstrak daun sisik naga. Hasil dari uji tanin dengan penambahan Fecl3 1% menghasilkan warna hijau kehitaman menandakan positif tanin pada ekstrak daun sisik naga. Hasil dari uji saponin dengan
penambahan aquadest lalu dikocok menghasilkan busa 1,5 cm menandakan adanya saponin pada ekstrak daun sisik naga. Hasil dari uji terpenoid/steroid dengan penambahan H2SO4 menghasilkan warna merah coklat menandakan adanya terpenoid pada ekstrak daun sisik naga (21).
Perbedaan hasil uji skining fitokimia pada penelitian sebelumnya dikarena beberapa factor salah satunya penggunakaan pelarut yang berbeda dengan konsentrasi berbeda, etanol merupakan pelarut yang bersifat universal sehingga mampu banyak menarik senyawa metabolit sekunder dibandingkan dengan methanol dan air, etanol 70% lebih polar dari pada etanol 96% (28).
Hasil Uji Organoleptis
Hasil uji organoleptis dapat dilihat pada tabel 4.
Tabel 4. Hasil Evaluasi Organoleptis Sediaan

Hasil Uji pH
Hasil pemeriksaan pH dapat dilihat pada tabel 5.
Tabel 5. Hasil Evaluasi pH Sediaan

Hasil Uji Viskositas
Hasil uji viskositas dapat dilihat pada tabel 6.
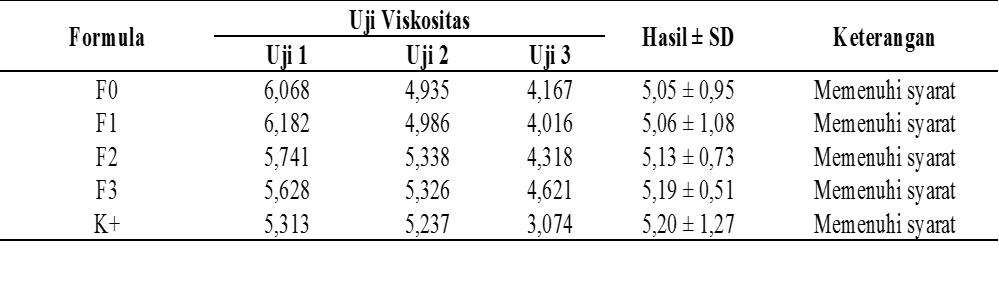
Tabel 6. Hasil Uji Viskositas Sediaan
Hasil Uji Stabilitas Sediaan
Hasil uji stabilitas sediaan dapat dilihat pada tabel 7.
Tabel 7. Hasil Uji Stabilitas


Berdasarkan tabel 7 bahwa stabilitas fisik sediaan obat kumur ekstrak daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) selama 6 siklus mengalami penurunan di setiap siklus, tetapi pada stabilitas fisik uji viskositas hasil nilai rata-rata yang diperoleh masih memenuhi syarat viskositas sediaan yaitu 1-7,25 cP. Faktor yang dapat mempengaruhi stabilitas produk farmasi yakni interaksi antara zat aktif dengan eksipien, proses sediaan dikemas, penyimpanan, dan jangka waktu dari pembuatan produk sampai pemakaian. Selain itu faktor lingkungan juga bisa mempengaruhi stabilitas seperti temperatur, radiasi, cahaya, dan udara.
Hasil Uji Antibakteri Sediaan Obat Kumur Terhadap Bakteri Streptococcus mutans dan Streptococcus viridans
Hasil uji antibakteri dapat dilihat pada tabel 8 dan tabel 9.
Tabel 8. Hasil Uji Antibakteri Sediaan Obat Kumur Terhadap Bakteri Streptococcus mutans
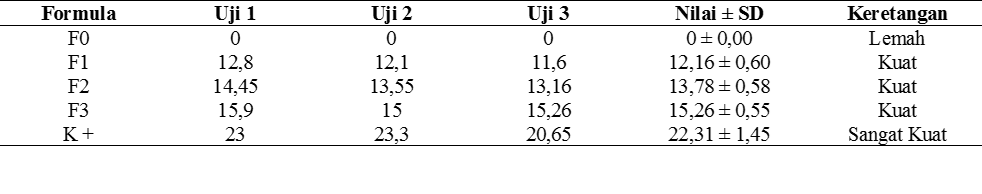
Tabel 9. Hasil Uji Antibakteri Sediaan Obat Kumur Terhadap Bakteri Streptococcus viridans
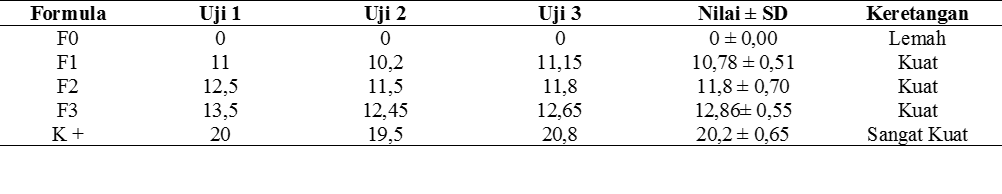
Keterangan :
F0 : Blanko
F1 : Obat kumur dengan ekstrak etanol daun sisik naga konsentrasi 5%
F2 : Obat kumur dengan ekstrak etanol daun sisik naga konsentrasi 10%
F3 : Obat kumur dengan ekstrak etanol daun sisik naga konsentrasi 15%
K+ : Obat kumur herbal enkasari
Hasil uji aktivitas antibakteri menujukan bahwa sediaan obat kumur ekstrak etanol daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) dapat menghambat pertumbuhan bakteri Streptococcus mutans dan Streptococcus viridans. Berdasrkan Kategori aktivitas respon hambatan pertumbuhan bakteri menurut (Davis & Stout) pada
zona hambat <5 mm kategori lemah, 5-10 mm kategori sedang, 10-20 mm katergori kuat, dan >20 mm kategori sangat kuat (30). Pada uji aktivitas antibakteri sediaan obat kumur ekstrak etanol daun sisik naga terhadapt bakteri Streptococcus mutans dengan konsentrasi 5% didapatkan zona hambat dengan rata-rata 12,16±0,60 mm, konsentrasi 10% didapatkan zona hambat dengan rata-rata 13,78±0,58 mm, konsentrasi 15% didapatkan zona hambat dengan rata-rata 15,25±0,55 mm dan pada k+ sebagai pembanding didapatkan zona hambat dengan rata-rata 22,31±1,45 mm. Pada uji aktivitas antibakteri sediaan obat kumur ekstrak daun sisik naga terhadap bakteri Streptococcus viridans dengan konsentrasi 5% didapatkan zona hambat dengan rata-rata 10,78±0,51 mm, konsentrasi 10% didapatkan zona hambat dengan rata-rata 11,8±0,70 mm, konsentrasi 15% didapatkan zona hambat dengan rata-rata 12,86±0,55 mm dan K+ sebagai pembanding didiapatkan zona hambat dengan rata-rata 20,2±0,65 mm.
Berdasarkan kategori zona hambat bakteri, konsentrasi 5%, konsentrasi 10%, dan konsentrasi 15% pada bakteri Streptococcus mutans termasuk ke dalam kategori kuat, pada konsentrasi 5%, konsentrasi 10%, konsentrasi 15% pada bakteri Streptococcus viridans termasuk ke dalam kategori kuat dengan ukuran zona hambat yang berbeda. Salah satu factor yang mempengaruhi zona hambat adalah konsentrasi.
Pada penelitian sebelumnya oleh (Ulfa, 2013), pengujian Aktivitas Antibakteri Dan KLT Bioautografi Ekstrak Etanol Daun Sisik Naga (Drymoglossum piloselloides) Terhadap Streptococcus mutans” dimana pada uji KLT konsentrasi 12,5 diketahui adanya hambatan terhadap S. mutans yang ditandai oleh daerah bening dengan diameter rata-rata 16,5 mm terlihat pada titik penotolan ekstrak (14). Pada penelitian (Haninah,dkk 2014), Uji antibakteri terhadap Streptcoccus viridans dengan konsentasi ekstrak etanol daun sisik naga 0,01%, 0,1%, 1% mempunyai zona hambat 5,35 mm, 5,73 mm, 6,19 mm (6). Pada penelitian (wirdarni L, 2021) hasil dari ektrak etanol daun sisik naga pada uji antibakteri dengan konsentrasi 10% dengan rata-rata zona hambat 11,21 mm pada Staphylococcus aureus (31).
Senyawa antibakteri merupakan senyawa kimiawi atau biologis baik alami maupun sintesik yang dapat menghambat pertumbuhan dan aktivitas bakteri. Aktivitas antibakteri pada penelitian ini menggunakan metode difusi dengan cara kertas cakram sebagai media untuk menyerap bahan antimikroba, setelah itu kertas cakram diletakkan pada permukaan media agar yang telah diinokulasi dengan biakan mikroba uji, kemudian diinkubasi selama 24 jam dengan suhu 37°C. Kelebihan dari metode cakram yaitu dapat dilakukan pengujian dengan lebih cepat pada penyiapan cakram, Hasil pengamatan yang diperoleh berupa ada tidaknya daerah bening yang terbentuk disekeliling kertas cakram yang menunjukan zona hambat pada pertumbuhan, pengukuran zona hambat menggunakan jangka sorong (9).
Hambatan yang dihasilkan sediaan obat kumur ekstrak daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) dikarenakan pada skrining fitokimia ekstrak daun sisik naga memiliki kandungan senyawa metabolit sekunder yaitu berupa alkaloid, flavonoid, tanin, saponin dan terpenoid, dimana senyawa metabolit sekunder tersebut mempunyai manfaat sebagai antibakteri. Flavonoid merupakan golongan senyawa fenol yang mempunyai sifat merusak membrane sitoplasma dan dapat menyebabkan kebocoran inti sel, tanin dapat merusak membrane dinding sel, terpenoid sebagai antibakteri dengan merusak porin pada membrane sel bakteri sehingga mengakibatkan sel abkteri akan kekurangan nutrisi (6). Mekanisme kerja alkaloid yaitu menghambat pembentukan sintesis protein sehingga dapat mengganggu metabolisme bakteri dan mengganggu komponen penyusun peptidoglikan pada lapisan dinding sel sehinnga menyebabkan kematian (32).
KESIMPULAN
Ekstrak etanol daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) dapat diformulasikan dalam sediaan obat kumur. Sediaan obat kumur ekstrak etanol daun sisik naga (Drymoglossum piloselloides (L.) C. Presl) memiliki aktivitas daya hambat pertumbuhan pada bakteri Streptococcus mutans dengan konsentrasi 5%, 10%, 15% zona hambat 12,16±0,60, 13,78±0,58 mm, 15,26±0,55 mm. Pada bakteri Streptococcus viridans dengan konsentrasi 5%, 10%, 15% zona hambat 10,78±0,51 mm, 11,8±0,70 mm, 12,86±0,55 mm. Dan konsentrasi optimum didapatkan pada konsentrasi 10% dan 15% pada Streptococcus mutans 13,78±0,58 mm, 15,26±0,55 mm dan pada Streptococcus viridans 11,8±0,70 mm, 12,86±0,55 mm.
Daftar Pustaka
- Marthinu LT, Bidjuni M. Penyakit Karies Gigi Pada Personil Detasemen Gegana Satuan Brimob Polda Sulawesi Utara Tahun 2019. JIGIM (Jurnal Ilmu Gigi dan Mulut). 2020;3(2):58–64.
- Fitri Handayani, Husnul Warnida SJN. Formulasi Dan Uji Aktivitas Antibakteri Streptococcus mutans Dari Sediaan Mouthwash Ekstrak Daun Salam (Syzygium polyanthum (Wight) Walp.). Jrnalu Chemistry. 2016;9(April):74–84.
- Nugraheni H, Sadimin S, Sukini S. Determinan Perilaku Pencegahan Karies Gigi Siswa Sekolah Dasar Di Kota Semarang. Jurnal Kesehatan Gigi. 2019;6(1):26.
- Suryani N, Adini S, Stiani NS, Indriatmoko DD. Obat Kumur Herbal Yang Mengandung Ekstrak Etil Asetat Kulit Batang Bintaro (Cerberra Odollam Gaertn) Sebagai Antibakteri Streptococcus Mutans Penyebab Plak Gigi. Farmaka. 2019;17(Vol 17, No 2 (2019): Farmaka (Agustus)):48–56.
- Khairani K, Busman B, Edrizal E. Uji Aktivitas Antibakteri Ekstrak Jamur Tiram Purih (Pleurotus Ostreatus) Terhadap Bakteri Streptococcus Mutans Penyebab Karies Gigi. B-Dental, Jurnal Kedoktan Gigi Universitas Baiturrahmah. 2019;4(2):110–6.
- Haninah, Lestari PE, Wahyukundari MA. Daya Antibakteri Ekstrak Daun Sisik Naga (Drymoglossum piloselloides [L.] Presl.) terhadap Streptococcus viridans. Artikel Ilmiah Hasil Penelitian Mahasiswa . 2014;
- A Buchari. 2018. Gerakan Masyarakat Hidup Sehat Dalam Mencegah Terjadinya Penyakit gigi dan mulut I Wayan Suanda. 2018;6(1):29–34.
- Pane M. Formulasi Sediaan Obat Kumur Ekstrak Teh Hijau (Camellia sinensis (L.) Kuntze). Univ Sumatera Utara. 2019;1.
- Nurhayati LS, Yahdiyani N, Hidayatulloh A. Perbandingan Pengujian Aktivitas Antibakteri Starter Yogurt Dengan Metode Difusi Sumuran Dan Metode Difusi Cakram. Jurnal Teknologi Hasil Peternakan. 2020;1(2):41.
- Sagita D, Ichwani MN. Riset Informasi Kesehatan, Vol. 6, No. 2 Desember 2017 Skrining aktifitas antibakteri dari ekstrak Sisik Naga ( Pyyrosia piloselloides (L) M.G.Price). 2017;6(2):115–9.
- Hamzah A. Analisis In Vitro Aktivitas Antibakteri Daun Sisik Naga (Drymoglossum pilosellaoides) Terhadap Bakteri Vibrio harveyi Dan Vibrio parahaemolyticus. Jurnal Aquac Fish Heal. 2019;8(2):86.
- Bali FA, Wehantouw F. Toksisitas Karakterisasi Gugus Fungsi Daun Sisik Naga ( Drymoglossum piloselloides ( L ) Presl .). Jurnal Ilmu Farmasi. 2014;3(3):335–41.
- Diana Febriani, Dina Mulyati, Endah Rismawati. Karakterisasi Simplisia dan Ekstrak Etanol Daun Sirsak (Annona muricata Linn). Peneliti Unisba. 2015;475–80.
- Ulfa EU, Sari DS, Wijaya D. Aktivitas Antibakteri Dan KLT Bioautografi Ekstrak Etanol Daun Sisik Naga (Drymoglossum piloselloides) Terhadap Streptococcus mutans. Stomatognatic-Jurnal Kedoktan Gigi. 2015;10(1):39–43.
- Fahmi A, Marpaung L, Bulan R. Uji Aktivitas Antioksidan dan Antibakteri dari Ekstrak Kasar Metanol Daun Sisik Naga ( Drymoglossum piloselloides ( L ) Presl ). 2017;2(1):1–12.
- Nashrianto DH, Dra MS, Aminingsih T, Si M, Matematika F, Alam P, et al. Identifikasi Senyawa Dalam Ekstrak Etanol Dan Fraksi Etil Asetat Daun Sisik Naga (Drymoglossum Piloselloides) Dengan Gc-Ms Dan Uji Aktivitas Antibakteri.
- Mayasari U, Laoli MT. Karakterisasi Simplisia Dan Skrining Fitokimia Daun Jeruk Lemon ( Citrus limon ( L .) Burm . f .). 2018;2(1):7–13.
- Anggraini T S. Pembuatan Tablet Ekstrak Daun Jambu Biji (Psidium guajava L) dan Di Kombinasikan dengan Ekstrak Rimpang Kunyit (Curcuma longa L) Dengan Variasi Bahan Pengikat Menggunakan Metode Granulasi Basah. 2019;
- Surbakti Chemayanti, Abadi Hafizhatul, Fitri Khairani D. Penuntun Praktikum Farmakognosi I. Medan; 2020.
- Fitri khairani, dkk. Penuntun Praktikum Fitokimia. Medan: Yayasan Helvetia; 2017. 74 p.
- Marjoni R. Dasar-Dasar Fitokimia. Jakarta: Penerbit Buku Kesehatan; 2016. 6–13 p.
- Loyd V AJ. ilmu & teknologi peracikan sediaan farmasi. Jakarta : EGC; 2018. 264 p.
- Fitria Fajar.R D k. . Formulasi sediaan obat kumur yang mengandung ekstrak herba tespong (oenanthe javanica dc) sebagai pencegah bau mulut. 2021;2(1):1–8.
- Noval N, Melviani M, Novia N, Syahrina D. Formulasi Dan Evaluasi Sediaan Obat Kumur (Mouthwash) Dari Ekstrak Etanol Tanaman Bundung (Actinoscirpus Grossus) Sebagai Antiseptik Mulut. J Surya Med. 2020;6(1):112–20.
- Izzaty RE, Astuti B, Cholimah N. Formulasi dan Uji Stabilitas Fisik Sediaan Gel Ekstrak Kulit Buah Rambutan. Angew Chemie Int Ed 6(11), 951–952. 1967;5:5–24.
- Octaviani M, Fadhli H, Yuneistya E. Antimicrobial Activity of Ethanol Extract of Shallot (Allium cepa L.) Peels Using the Disc Diffusion Method. Pharmacy Sci Res. 2019;6(1):62–8.
- Depkes R. Materia Medika Indonesia Jilid I. Jakarta: Departemen Kesehatan RI; 1977.
- Riwanti P, Izazih F, Amaliyah A. Pengaruh Perbedaan Konsentrasi Etanol pada Kadar Flavonoid Total Ekstrak Etanol 50,70 dan 96% Sargassum polycystum dari Madura. Jurnal Pharmacy Anwar Medan. 2018;2(2):35–48.
- Harun N, Febrianti S E. Uji Efektivitas Antiseptik Obat Kumur Ekstrak Daun Sirih Hijau (Piper betle L.) Terhadap Bakteri Isolat Mulut. Jurnal Sains dan Kesehatan. 2022;4(3):268–74.
- Davis WW, Stout TR. Disc Plate Method of Microbiological Antibiotic Assay. Appl Microbiol. 1971;22(4):659–65.
- Widarni L. Uji Aktivitas Antimikroba Ekstrak Etanol Sisik Naga (Pyrrosia piloselloides (L.) M.G. Price) Terhadap Bakteri Staphylococcus aureus, Salmonella typhi Dan Jamur Candida albicans. jurnal Farmasi, Institut Kesehatan Helvetia, Medan. 2021. 118 p.
- Anggraini W, dkk. Aktivitas antibakteri ekstrak etanol 96 % buah blewah (cucumis melo l . Var . Antibacterial activity of 96 % ethanol extract cantaloupe fruit ( cucumis melo l . Var . Cantalupensis ) against escherichia coli bacteria. Pharmacy Jurnal Indonesia. 2019;5(1):61–6.
cara mengutip artikel ini
https://jurnal.unpad.ac.id/farmasetika/rt/captureCite/46118/0
 Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3
Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3


