Majalah Farmasetika, 7 (5) 2022, 424-458 https://doi.org/10.24198/mfarmasetika.v7i5.39510
Artikel Review
Download PDF
Rizqa Nurul Aulia*1, Sriwidodo2
1Program Studi Magister Ilmu Farmasi, Fakultas Farmasi, Universitas Padjadjaran
2Departemen Teknologi Farmasi dan Farmasi, Fakultas Farmasi, Universitas Padjadjaran, Jl. Raya Bandung Sumedang km 21 Jatinangor 45363, Jawa Barat, Indonesia
*Email: rizqa16001@mail.unpad.ac.id
(Submit 30/05/2022, Revisi 03/06/2022, Diterima 26/06/2022, Terbit 21/07/2022)
Abstrak
Penggunaan bahan alam dalam dunia kesehatan telah banyak dipilih secara turun temurun untuk menangani berbagai macam masalah kesehatan. Namun penggunaan tanaman sebagai zat aktif dalam formulasi obat masih memiliki banyak keterbatasan terutama dalam kelarutan dan bioavailibilitas dalam tubuh. Untuk mengatasi hal tersebut, penelitian terkait sistem penghantaran obat herbal terus dikembangkan dengan tujuan untuk membuat formulasi terbaik dan tercapainya efektivitas terapi dari obat herbal. Sistem penghantaran baru obat herbal antara lain meliputi sistem penghantaran vesikular seperti liposom, fitosom, etosom, transferosom, penghantaran partikulat seperti mikrosfer, nanopartikel. Penggunaan sistem penghantaran obat tersebut bertujuan meningkatkan stabilitas, ketersediaan hayati dan pengurangan toksisitas. Tinjauan ini menyoroti status perkembangan formulasi herbal baru dan aplikasinya dalam terapi.
Kata Kunci
Sistem penghantaran obat, obat herbal, aplikasi biomedik
Pendahuluan
Penggunaan bahan alam masih menjadi pilihan yang dipercaya secara turun temurun dan secara luas memiliki kebermanfaatan, terutama penggunaannya sebagai zat aktif dalam pengobatan1,2. Pengobatan dengan tanaman tradisional diharapkan mampu memberikan manfaat yang sama besar namun memiliki efek samping yang lebih rendah dari obat sintesis3. Namun penggunaan tanaman sebagai zat aktif dalam formulasi obat masih memiliki banyak keterbatasan diantaranya adalah kelarutan, biovailibilitas yang kurang baik dalam tubuh, ketidakstabilan dalam pH asam lambung, metabolisme pra sistemik di hati, kelarutan dan masalah penyerapan dalam tubuh, semua hal ini dapat menyebabkan tingkat obat di bawah konsentrasi terapeutik dalam plasma, hal ini menyebabkan kurang atau tidak ada efek terapeutik dari obat herbal tersebut4 Sehingga untuk mengatasi hal tersebut, penelitian terkait sistem penghantaran obat herbal terus dikembangkan dengan tujuan untuk membuat formulasi terbaik dan tercapainya efektivitas terapi dari obat herbal tersebut5. Penggunaan teknologi pengiriman obat untuk tanaman aktif, terbukti dapat meminimalkan metabolisme prasistemik, degradasi obat di saluran pencernaan, distribusi/akumulasi obat di non jaringan dan organ target serta mengurangi efek samping dan meningkatkan kemanjuran terapi6. Sistem penghantaran obat baru herbal ini meliputi sistem penghantaran vesikular seperti liposom, fitosom, etosom, transferosom, sistem penghantaran partikulat seperti mikrosfer, mikropellet, nanopartikel, dan emulsi mikro dan nano7. Artikel ini akan membahas terkait sistem penghantaran obat yang digunakan untuk memuat dalam formulasi obat dengan ekstrak tanaman.

Hasil
Sistem Penghantaran Obat baru untuk Obat Herbal
Berdasarkan data yang diperoleh dari penelitian terbaru, dilaporkan bahwa lebih dari 70% obat herbal yang diformulasikan dengan metode konvensional menunjukkan adanya masalah stabilitas, kelarutan pada lipid yang rendah, keterbatasan bioavailabilitas, stabilitas yang buruk terhadap asam lambung, metabolisme yang buruk oleh efek mikroflora usus dan penyerapan yang buruk di dinding usus, factor ini juga yang menyebabkan sering terjadinya kegagalan dalam uji klinis pada penelitian obat herbal8,9 . Penelitian terkait sistem penghantaran obat untuk obat herbal terus dilakukan,
Sistem penghantaran obat baru yang digunakan untuk obat herbal harus dapat memastikan zat aktif obat herbal ke tempat kerjanya dengan kecepatan yang dapat dimodifikasi sesuai dengan kebutuhan tubuh atau farmakologi dari penyakit, selama periode pengobatan10. Berbagai sistem penghantaran obat baru yang telah digunakan untuk obat herbal dan fitokimia dapat secara luas diklasifikasikan ke dalam kelompok berikut11.
1.Sistem penghantaran vesikular, yang meliputi liposom, fitosom, etosom, transferosom.
2.Sistem penghantaran partikulat, yang meliputi mikrosfer dan nanopartikel-
Sistem Penghantaran Vesikular
Liposom
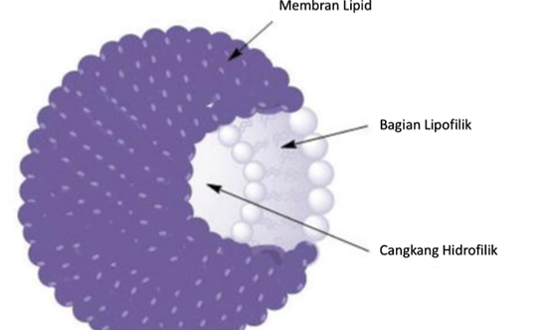
Liposom adalah sistem penghantaran obat biodegradable, koloid dengan bentuk bulat dengan diameter 0,05-5,0 m, terdiri dari membran lipid bilayer yang menjebak inti berair12. Istilah liposom berasal dari dua kata Yunani: “Lipos” berarti gemuk dan “Soma” berarti tubuh13. Liposom adalah vesikel terbuat dari bahan yang sama dari sel selaput. Biasanya ini terdiri dari fosfolipid, molekul yang terdiri ekor dan bagian kepala14. keuntungan yang diterima dari penggunaan liposom yaitu peningkatan kelarutan, indeks terapeutik, mencapai kemampuan untuk menargetkan organ, mengurangi toksisitas dan resistensi multikomponen15. Beberapa penelitian menunjukkan bahwa untuk obat herbal yang diformulasikan menjadi liposom memberikan hasil yang baik dengan adanya peningkatan stabilitas, biovailibilitas dan penurunan efek samping16,17. Struktur Liposom dapat dilihat pada Gambar 218. Beberapa obat herbal yang diformulasikan menjadi liposom sebagai sistem penghantaran obat, disebutkan pada Tabel 119,20,21,22,23.

Tabel 1. Sistem penghantaran liposom pada ekstrak herbal

Fitosom
Phyto-phospholipid Complex atau dikenal sebagai fitosom merupakan komplek yang terbuat dari ikatan hydrogen antara fitokonstituen dengan fosfolipid yang mampu menunjang stabilitas fisik dan menunjang absorbsi obat herbal24. Dalam fitosom, kompleksasi fosfolipid dan komponen tanaman aktif yang larut dalam air melibatkan pembentukan ikatan kimia dan karenanya lebih stabil. Sedangkan pada liposom tidak


terbentuk ikatan kimia; molekul fosfatidilkolin hanya mengelilingi komponen yang larut dalam air25. Perbedaan fitosom dan liposom terletak pada terjadinya ikatan kimia antara fosfotidilkolin dengan obat dalam sistem penghantaran obat tersebut. Beberapa obat herbal yang diformulasikan menjadi fitosom sebagai sistem penghantaran obat, disebutkan pada Tabel 226,27,28,29,30,31.
Tabel 2. Sistem penghantaran fitosom pada ekstrak herbal

Etosom
Etosom adalah vesikel yang terdiri dari fosfolipid dan konsentrasi etanol yang tinggi32. Konsentrasi etanol yang tinggi dalam etosom meningkatkan permeabilitasnya melalui kulit dengan fluidisasi lipid kulit33,34. Pembawa ini dapat menembus kulit secara mendalam yang mengarah pada peningkatan pengiriman obat ke dalam lapisan kulit yang lebih dalam dan bahkan ke dalam sirkulasi darah35. Beberapa obat herbal yang diformulasikan menjadi ftosom sebagai sistem penghantaran obat, disebutkan pada Tabel 336,37,38.
Tabel 3. Sistem penghantaran Etosom pada ekstrak herbal

Transferosom
Transferosom adalah vesikel fosfolipid yang terutama digunakan sebagai pembawa untuk pengiriman obat secara transdermal. Formulasi transferosom meliputi fosfolipid yang bertindak sebagai bahan pembentuk vesikel, surfaktan untuk memberikan fleksibilitas, alkohol sebagai pelarut dan zat penyangga sebagai media pembasah39,40. Beberapa penelitian juga menyebutkan bahwa penggunaan transferosome ini menghasilkan penyerapan yang lebih baik41,42. Beberapa obat herbal yang diformulasikan menjadi Transferosome sebagai sistem penghantaran obat, disebutkan pada Tabel 443,44,45.
Tabel 4. Sistem penghantaran Transferosom pada ekstrak herbal

Sistem Penghantaran Partikulat
Mikrosfer dan Mikrokapsul
Mikrosfer adalah partikel bulat berukuran 1-1000 m, di mana obat terdispersi secara merata dalam matriks polimer dan dilepaskan mengikuti kinetika orde pertama. Penggunaan polimer mikrosfer dan mikrokapsul sebagai pembawa zat aktif memungkinkan untuk mencapai pelepasan terkontrol atau berkelanjutan, perbedaan keduanya terlihat pada bentuk mikrosfer yang tidak memiliki dinding atau selubung yang jelas terlihat46,47. Penggunaan pembawa seperti mikrosfer dan mikrokapsul sarat dengan ekstrak herbal karena dapat mengatasi keterbatasan formulasi konvensional dengan meningkatkan kelarutan, aktvitas farmakologis dan bioavailabilitas48,49. Beberapa obat herbal yang diformulasikan menjadi Mikrosfer dan Mikrokapsul sebagai sistem penghantaran obat, disebutkan pada Tabel 550,51,52,53.
Tabel 5. Sistem penghantaran Mikrosfer dan Mikrokapsul pada ekstrak herbal


Nanopartikel
Nanopartikel adalah partikel berukuran submikron berdiameter sekitar 200 nm yang terdiri dari polimer yang dapat terurai dan tidak dapat terurai. Keuntungan dari nanopartikel termasuk peningkatan stabilitas, penyimpanan jangka panjang, peningkatan kelarutan komponen, peningkatan penyerapan obat yang dimasukkan dan pengurangan dosis dan efek samping terkait dosis. Nanopartikel dapat digunakan untuk pelepasan terkontrol serta untuk menargetkan obat ke jaringan atau organ tertentu54. Beberapa obat herbal yang diformulasikan menjadi Nanopartikel sebagai sistem penghantaran obat, disebutkan pada Tabel 655,56,57..
Tabel 6. Sistem penghantaran Mikrosfer dan Mikrokapsul pada ekstrak herbal


Kesimpulan
Penggunaan tanaman herbal sebagai obat ini merupakan jawaban dari kekhawatiran terkait efek samping yang ditimbulkan oleh obat sintesis namun memiliki efek terapi yang mendekati atau sama dengan obat sintesis. Penerapan sistem penghantaran obat baru untuk obat herbal telah digunakan untuk tujuan peningkatan bioavailabilitas, peningkatan kelarutan dan permeabilitas yang masih menjadi permasalahan dari obat herbal. Namun, dengan adanya sistem penghantaran yang tepat maka akan menjadi solusi dari permasalahan terebut. Beberapa penelitan dilaporkan bahwa banyak tanaman yang telah menunjukkan efek terapeutik yang meningkat pada dosis yang sama atau kurang ketika dimasukkan ke dalam sistem penghantaran obat baru dibandingkan dengan ekstrak dengan metode konvensional. Penggunaan teknologi pengiriman obat untuk obat herbal telah terbukti dapat meminimalkan metabolisme prasistemik, degradasi obat di saluran pencernaan, distribusi/akumulasi obat di non jaringan dan organ target serta mengurangi efek samping dan meningkatkan kemanjuran terapi. Oleh karena itu, ada potensi besar dalam pengembangan sistem penghantaran obat baru untuk obat-obatan herbal sebagai pilihan obat dalam berbagai macam terapi.
Daftar Pustaka
- Luo, H., Vong, C.T., Chen, H. et al. 2019. Naturally occurring anti-cancer compounds: shining from Chinese herbal medicine. Chin Med 14, 48. https://doi.org/10.1186/s13020-019-0270-9
- WHO. Progress Report by the Director General. Geneva: World Health Orgaanization; 1991 Mar. Report No.: 444/20-22
- Chavda VP, Ertas YN, Walhekar V, Modh D, Doshi A, Shah N, et al. 2021. Advanced Computational Methodologies Used in the Discovery of New Natural Anticancer Compounds. Front Pharmacol. 12:702611. doi:10.3389/fphar.2021.702611
- Welz, A.N., Emberger-Klein, A. & Menrad, K. Why people use herbal medicine: insights from a focus-group study in Germany. BMC Complement Altern Med 18, 92 (2018). https://doi.org/10.1186/s12906-018-2160-6
- Ong YS, Saiful Yazan L, Ng WK, et al. Thymoquinone loaded in nanostructured lipid carrier showed enhanced anticancer activity in 4T1 tumor-bearing mice. Nanomedicine. 2018;13(13):1567–1582. doi:10.2217/nnm-2017-0322
- Hajialyani, M., Tewari, D., Sobarzo-Sánchez, E., Nabavi, S. M., Farzaei, M. H., & Abdollahi, M. (2018). Natural product-based nanomedicines for wound healing purposes: therapeutic targets and drug delivery systems. International journal of nanomedicine, 13, 5023–5043. https://doi.org/10.2147/IJN.S174072
- Awad A, Al-Shaye D. Public awareness, patterns of use and attitudes toward natural health products in Kuwait: a cross-sectional survey. BMC Complement Altern Med. 2014; [cited 2017 Apr 11]; 14. Available from: http://bmccomplementalternmed.biomedcentral.com/articles/10.1186/1472- 6882-14-105.
- Chauhan P, Tyagi BK. Herbal novel drug delivery systems and transferosomes. J Drug Delivery Ther. 2018;8(3):162–168. doi:10.22270/jddt.v8i3.1772
- Sandhiya, V., Ubaidulla, U. A review on herbal drug loaded into pharmaceutical carrier techniques and its evaluation process. Futur J Pharm Sci 6, 51 (2020). https://doi.org/10.1186/s43094-020-00050-0
- Rohilla R, Garg T, Goyal AK, Rath G. Herbal and polymeric approaches for liver- targeting drug delivery: novel strategies and their significance. Drug Deliv. 2016;23(5):1645–1661. doi:10.3109/ 10717544.2014.945018
- Thomford, N.E.; Senthebane, D.A.; Rowe, A.; Munro, D.; Seele, P.; Maroyi, A.; Dzobo, K. Natural Products for Drug Discovery in the 21st Century: Innovations for Novel Drug Discovery. Int. J. Mol. Sci. 2018, 19, 1578. https://doi.org/10.3390/ijms19061578
- Ben-Shabat, S., Yarmolinsky, L., Porat, D. et al. Antiviral effect of phytochemicals from medicinal plants: Applications and drug delivery strategies. Drug Deliv. and Transl. Res. 10, 354–367 (2020). https://doi.org/10.1007/s13346-019-00691-6
- Salunkhe, V. R., Patil, P. S., Wadkar, G. H. and Bhinge, S. D. (2021) “Herbal Liposomes: Natural Network for Targeted Drug Delivery System”, Journal of Pharmaceutical Research International, 33(29B), pp. 31-41. doi: 10.9734/jpri/2021/v33i29B31586.
- Sharma P, Verma S, Misri P, Global need for novel herbal drug formulations, Int. J. Pharmacog. Phytochem. Res. 2016;8:1535-1544.
- Samad A, Sultana Y, Aqil M. Liposomal drug delivery systems: An update review, Curr. drug deliv. 2007;4:297-305.
- Verma N, Roshan A, liposomes: A targeted drug delivery system, AMS. 2015;2:65-70.
- Singh RP, Singh SG, Naik H, Jain D, Bisla S (2014) Herbal excipients in novel drug delivery system. Int J Comprehensive Pharm 2:1–7
- Gregoriadis, Gregory. 2017. Liposome Technology. 1st edition. England : CRC Press.
- Aslan, İ. & Kurt, A. A. (2021). In-vitro comparison release study of novel liposome and conventional formulation containing Rosmarinus officinalis extract . Current Perspectives on Medicinal and Aromatic Plants (CUPMAP) , 4 (1) , 13-21 . DOI: 10.38093/cupmap.848115
- Chen, Jun & Zhang, Ting & Cai, Baochang & Chen, Minglei & Fang, Yun. 2010. Pharmaceutical properties of novel liposomes containing total alkaloids from seed of Strychnos nux-vomica. Zhongguo Zhong yao za zhi = Zhongguo zhongyao zazhi = China journal of Chinese materia medica. 35. 35-9. 10.4268/cjcmm20100107.
- Di Costanzo, A., & Angelico, R. 2019. Formulation Strategies for Enhancing the Bioavailability of Silymarin: The State of the Art. Molecules (Basel, Switzerland), 24(11), 2155. https://doi.org/10.3390/molecules24112155
- Al-Samydai, A., Alshaer, W., Al-Dujaili, E., Azzam, H., & Aburjai, T. (2021). Preparation, Characterization, and Anticancer Effects of Capsaicin-Loaded Nanoliposomes. Nutrients, 13(11), 3995. https://doi.org/10.3390/nu13113995
- Singh, Aditya. Shubhrat maheshwari. 2020. Extraction, Development, and Characterization of Tamarind Seed Oil Based Liposome. International Journal of Pharmaceutical Research | Jul – Sep 2020 | Vol 12 | Issue 3
- W. He, Y. Du, W. Zhou, C. Yao, X. Li, Redox-sensitive dimeric camptothecin phosphatidylcholines-based liposomes for improved anticancer efficacy, Nanomedicine 14 (2019) 3057–3074.
- Amit P., Tanwar YS., Rakesh S., Poojan P. 2013. Phytosome : Phytolipid Drug Delivery System for Improving Bioavailability of Herbal Drug. J. Pharm. Sci. Biosci. Res. Vol 3(2): 51–57
- Ju Ho P, Jun Sung J, Ki Cheon K, Jin Tae H. Anti-inflammatory effect of Centella asiatica phytosome in a mouse model of phthalic anhydride-induced atopic dermatitis. Phytomedicine. 2018 Apr 1;43:110-119. doi: 10.1016/j.phymed.2018.04.013. Epub 2018 Apr 6. PMID: 29747743.
- Pastorelli, Davide; Fabricio, Aline S.C.; Giovanis, Petros; D’Ippolito, Simona; Fiduccia, Pasquale; Soldà, Caterina; Buda, Andrea; Sperti, Cosimo; Bardini, Romeo; Da Dalt, Gianfranco; Rainato, Giulia; Gion, Massimo; Ursini, Fulvio (2018). Phytosome complex of Curcumin as complementary therapy of advanced pancreatic cancer improves safety and efficacy of gemcitabine: Results of a prospective phase II trial. Pharmacological Research, (), S1043661818301609– . doi:10.1016/j.phrs.2018.03.013
- Di Pierro F, Khan A, Bertuccioli A, Maffioli P, Derosa G, Khan S, et al. Quercetin Phytosome® as a potential candidate for managing COVID-19. Minerva Gastroenterol 2021;67:190-5. DOI: 10.23736/S2724-5985.20.02771-3
- Rasaie, Solmaz., Saeed Ghanbarzadeh., Maryam Mohammadi., Hamed Hamishehkar. 2014. Nano Phytosomes of Quercetin: A Promising Formulation for Fortification of Food Products with Antioxidants. Pharmaceutical sciences, 2014, 20, 96-101
- Alharbi, Waleed S., Fahad A. Almughem., Alshaimaa M. Almehmady., Somayah J. Jarallah .,Wijdan K. Alsharif., Nouf M. Alzahrani 2 and Abdullah A. Alshehri. 2021 Phytosomes as an Emerging Nanotechnology Platform for the Topical Delivery of Bioactive Phytochemicals. Pharmaceutics 2021, 13, 1475
- Rimkiene, Laura., Juste Baranauskaite., Mindaugas Marksa., Laurynas Jarukas and Liudas Ivanauskas.2021. Development and Evaluation of Ginkgo biloba L. Extract Loaded into Carboxymethyl Cellulose Sublingual Films. Appl. Sci. 2021, 11(1), 270; https://doi.org/10.3390/app11010270
- Gangwar S, Singh S, Garg G. Ethosomes: A novel tool for drug delivery through skin. J Pharm Res. 2010; 3(4): 688-691.
- Singh, M. P., Nayak, A., & Pal, J. A. (2019). Ethosome: A Novel Approaches for Herbal Drug Delivery System. International Journal of Pharmacy & Life Sciences, 10(6).
- Pandey, Vikas, Dilip Golhani, and Rajesh Shukla. 2014. Ethosomes: versatile vesicular carriers for efficient transdermal delivery of therapeutic agents. Drug Delivery, Early Online: 1–15
- Solomon CU, Onuoha I (2013) Preliminary phytochemical screening of different solvent extracts of stems bark and roots of Dennetia tripetala. Asian J Plant Sci Res 3(3):10–13
- Sasindran, S., Easwaran, M., Shyamala, G., Karuppaiah, A., Siram, K., & Veintramuthu, S. (2019). Phytochemical screening and cytotoxicity evaluation of crude extracts: Toxicity comparison of crude extracts and its ethosomal formulations. Journal of Cosmetic Dermatology. doi:10.1111/jocd.13234
- Dewi, A. D. S. P., Jufri, M., & Iskandarsyah (2018). Development and In Vitro penetration test of ethosomal cream-containing pegagan (centella asiatica) herbal extract. International Journal of Applied Pharmaceutics, 10(Special Issue 1), 120-125. https://doi.org/10.22159/ijap.2018.v10s1.25
- Hyder, Imran & Naseer, Arif & Ahmad, Adil. (2021). In Vitro Assessment of Herbal Topical Ethosomal Gel Formulation for the Treatment of Acne vulgaris. Asian Pacific Journal of Health Sciences. 8. 10.21276/apjhs.2021.8.4.17.
- Chauhan P, Tyagi B. HERBAL NOVEL DRUG DELIVERY SYSTEMS AND TRANSFERSOMES. JDDT [Internet]. 2018 [cited 29May2022];8(3):162-8. Available from: http://www.jddtonline.info/index.php/jddt/article/view/1772
- Chen Rong-Ping, Chavda Vivek P., Patel Aayushi B., Chen Zhe-Sheng. 2022. Phytochemical Delivery Through Transferosome (Phytosome): An Advanced Transdermal Drug Delivery for Complementary Medicines. Frontiers in Pharmacology. Vol 12
- Ascenso, A., Raposo, S., Batista, C., Cardoso, P., Mendes, T., Praça, F. G., et al. (2015). Development, Characterization, and Skin Delivery Studies of Related Ultradeformable Vesicles: Transfersomes, Ethosomes, and Transethosomes. Int. J. Nanomedicine 10, 5837–5851. doi:10.2147/IJN.S86186
- Ikasari ED, Fudholi A, Martono S, Marchaban (2015) Compartemental modelling approach of floatingmucoadhesive nifedipine tablet in vitro and in vivo. Int J Pharma Sci Res 6(8): 1169–1178.
- Fitrya, Fitrya., Najma Annuria Fithri., Mesri Winda., Muharni Muharni. 2020. Ethanol extract of Parkia speciosa Hassk. loaded transfersome: Characterization and optimization. Journal of Pharmacy & Pharmacognosy Research, 8 (3), 167- 176, 2020 ISSN 0719-4250
- Nimisha, Rizvi, D. A., Fatima, Z., Neema, & Kaur, C. D. (2017). Antipsoriatic and Anti-inflammatory Studies of Berberis aristata Extract Loaded Nanovesicular Gels. Pharmacognosy magazine, 13(Suppl 3), S587–S594. https://doi.org/10.4103/pm.pm_210_17
- Hammed Tanimowo Aiyelabegan, Malihe Ebadi, Gholam Ali Kardar, Nasrin Lotfibakhshaiesh, Farid Abedin Dorkoosh, Somayeh Ebrahimi_Barough, Esmaeil Sadroddiny. (2020) k-Casein upregulates osteogenic differentiation on bone marrow mesenchymal stem cells cultured on agarose microcarriers. International Journal of Polymeric Materials 69:6, pages 373-380.
- Teekamp, N.; Van Dijk, F.; Broesder, A.; Evers, M.; Zuidema, J.; Steendam, R.; Post, E.; Hillebrands, J.L.; Frijlink, H.W.; Poelstra, K.; Beljaars, L.; Olinga, P.; Hinrichs, W.L.J. (2017). Polymeric microspheres for the sustained release of a protein-based drug carrier targeting the PDGFβ-receptor in the fibrotic kidney. International Journal of Pharmaceutics, 534(1-2), 229– 236. doi:10.1016/j.ijpharm.2017.09.072
- Xi Liang, Li Xie, Qingyuan Zhang, Ge Wang, Siyuan Zhang, Mingyan Jiang, Ruitao Zhang, Ting Yang, Xingyu Hu, Ziyang Yang, Weidong Tian, 2022. Gelatin methacryloyl-alginate core-shell microcapsules as efficient delivery platforms for prevascularized microtissues in endodontic regeneration, Acta Biomaterialia, Volume 144. Pages 242-257, ISSN 1742-7061, https://doi.org/10.1016/j.actbio.2022.03.045.
- Raj H, Sharma S, Sharma A, Verma K, Chaudhary A. A Novel Drug Delivery System: Review on Microspheres. JDDT [Internet]. 15Apr.2021 [cited 16Jun.2022];11(2-S):156-61. Available from: http://jddtonline.info/index.php/jddt/article/view/4792
- Agnihotri, Nitika & Mishra, Ravinesh & Goda, Chirag & Arora, Manu. (2012). Microencapsulation – A Novel Approach in Drug Delivery: A Review. Indo Global J Pharm Sci. 2. 1-20.
- Kozlowska, Justyna; Stachowiak, Natalia; Prus, Weronika (2019). Stability studies of collagen-based microspheres with Calendula officinalis flower extract. Polymer Degradation and Stability, 163(), 214– 219. doi:10.1016/j.polymdegradstab.2019.03.015
- Yousefi, Mojtaba; Khorshidian, Nasim; Mortazavian, Amir Mohammad; Khosravi- Darani, Kianoush (2019). Preparation optimization and characterization of chitosan-tripolyphosphate microcapsules for the encapsulation of herbal galactagogue extract. International Journal of Biological Macromolecules, doi:10.1016/j.ijbiomac.2019.08.122
- Suryavanshi, Vandana Singh; Maharana, Tungabidya, Jagtap, Pratik Kumar. 2022. Microencapsulation of Cassia Fistula Flower Extract with Chitosan and its Antibacterial Studies. Current Drug Delivery.
- Gyawali, R., Ghimire, A., Khatiwada, A., Niraula, P., Sharma, U., & Thapa, R. (2020). Anti-inflammatory, Anxiolytic and Antioxidant Property of Lactuca sativa L and Formulation of Microspheres Loaded Sustained Release Anti-inflammatory Gel. Journal of Nepal Chemical Society, 41(1), 8–15. https://doi.org/10.3126/jncs.v41i1.30371
- Moradi Seyed Zachariah, Momtaz Saeideh, Bayrami Zahra, Farzaei Mohammad Hosein, Abdollahi Mohammad. 2020. Nanoformulations of Herbal Extracts in Treatment of Neurodegenerative Disorders. Frontiers in Bioengineering and Biotechnology. Vol 8 DOI=10.3389/fbioe.2020.00238. ISSN=2296-4185
- Shahriari, Marjan; Veisi, Hojat; Hekmati, Malak; Nemmati, Saaba (2018). In situ green synthesis of Ag nanoparticles on herbal tea extract ( Stachys lavandulifolia )-modified magnetic iron oxide nanoparticles as antibacterial agent and their 4- nitrophenol catalytic reduction activity. Materials Science and Engineering: C, (), S0928493117337487–. doi:10.1016/j.msec.2018.04.044
- M. Bala Chennaiah;K. Dilip Kumar;B. Sudheer Kumar;Srinivasa Rao Tanneeru; (2021). Characterisation of zinc oxide nanoparticles–herbal synthesised coated with cimum tenuiflorum advances in Materials and Processing Technologies, (), – . doi:10.1080/2374068x.2021.1934642
- Yang, B., Jiang, J., Jiang, L., Zheng, P., Wang, F., Zhou, Y. Wang, Q. (2020). Chitosan mediated solid lipid nanoparticles for enhanced liver delivery of zedoary turmeric oil in vivo. International Journal of Biological Macromolecules, 149, 108– 115. doi:10.1016/j.ijbiomac.2020.01.2
Cara mengutip artikel ini
 Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3
Majalah Farmasetika Jurnal Ilmiah Nasional Terakreditasi SINTA 3